
Δρ
Καραγκούνη Ευδοκία
Η ομάδα Ανοσολογίας Λοίμωξης ανήκει στο Εργαστήριο Κυτταρικής Ανοσολογίας του Τμήματος Μικροβιολογίας του ΕΙΠ και δραστηριοποιείται στο πεδίο των παρασιτικών λοιμώξεων. Ειδικότερα, το ερευνητικό ενδιαφέρον της ομάδας εστιάζεται:
- στην ανάλυση των μηχανισμών ανοσοπαθογένειας που καθορίζουν την ανάπτυξη του νοσήματος, με στόχο τον προσδιορισμό βιομορίων για την ανάπτυξη ανοσοθεραπειών και
- στον προσδιορισμό μακρομορίων ή αντιγονικών καθοριστών του παθογόνου με δυνατότητα αξιοποίησης στην ανάπτυξη εμβολίων ή διαγνωστικών.
Τα τελευταία χρόνια, έχουμε αναπτύξει τεχνογνωσία στην κατασκευή πεπτιδικών εμβολίων, τα οποία χορηγούμενα με βιοαποικοδομήσιμους νανοφορείς έχουν την ικανότητα να επάγουν προστασία σε πειραματικά μοντέλα σπλαχνικής λεϊσμανίασης. Παράλληλα, αναλύοντας τους υποκείμενους ανοσολογικούς μηχανισμούς που διέπουν την προστασία έναντι της ευαισθησίας στη μόλυνση, έχει προσδιοριστεί ένα σύνολο βιοδεικτών, οι οποίοι μπορούν να χρησιμοποιηθούν ως μοριακοί στόχοι για ανοσοπαρέμβαση, ενισχύοντας την αποτελεσματικότητα των υποψηφίων εμβολίων.
A. Ανοσολογία Λεϊσμανίασης και Ανάπτυξη Εμβολίων
Η λεϊσμανίαση είναι ένα σύμπλεγμα νοσημάτων που μεταδίδονται με έντομα και οφείλονται σε πρωτοζωικά παράσιτα του γένους Leishmania. Η προμαστιγωτή μορφή του παρασίτου μεταδίδεται με το δήγμα μολυσμένων φλεβοτόμων, η οποία μετασχηματίζεται στην αμαστιγωτή μορφή και πολλαπλασιάζεται εντός των φαγοκυττάρων του ξενιστή (θηλαστικά, πχ άνθρωπος, σκύλος). Οι κλινικές εκφάνσεις της νόσου κυμαίνονται από ιάσιμες, ασυμπτωματικές μολύνσεις έως εντοπισμένες αλλοιώσεις του δέρματος, ενώ δύναται να αναπτυχθεί η σπλαχνική μορφή της νόσου, η οποία είναι θανατηφόρος εάν δεν χορηγηθεί θεραπεία. Σύμφωνα με επιδημιολογικά στοιχεία, η σπλαχνική λεϊσμανίαση είναι η δεύτερη πιο συχνή αιτία θανάτου μεταξύ των παρασιτικών λοιμώξεων που πλήττουν κυρίως τους φτωχούς ανθρώπους στις τροπικές και υποτροπικές περιοχές του κόσμου. Παρά το γεγονός, ότι πολλές κλινικές μελέτες δείχνουν ότι η προστασία έναντι του νοσήματος μπορεί να επιτευχθεί στο μεγαλύτερο μέρος του πληθυσμού μέσω εμβολιασμού και ότι ένας σημαντικός αριθμός υποψηφίων εμβολίων έχει αξιολογηθεί με επιτυχία σε ζωικά μοντέλα του νοσήματος, εξακολουθεί να μην υπάρχει αποτελεσματικό εμβόλιο για τον άνθρωπο. Τα τελευταία χρόνια, προσεγγίσεις εμβολιολογίας συστημάτων έχουν συμβάλλει τόσο στην κατανόηση της παθογένειας της λεϊσμανίασης, όσο και των μηχανισμών ανάπτυξης προστατευτικής ανοσίας, ανοίγοντας νέες οδούς στην έρευνα των εμβολίων.
Α1. Κατασκευή PLGA νανοεμβολίων για αποτελεσματική στόχευση των δενδριτικών κυττάρων
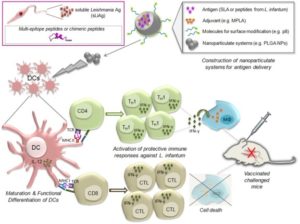 Η ικανότητα του εκάστοτε εμβολίου να εγείρει τις επιθυμητές ανοσολογικές αποκρίσεις εξαρτάται όχι μόνο από το περιελαμβανόμενο αντιγόνο και ανοσοενισχυτικό, αλλά και από τις μορφολογικές ιδιότητες και το μέγεθος του ίδιου του εμβολίου. Τα τελευταία χρόνια η ανάπτυξη των νανο-εμβολίων θεωρείται μία από τις πιο επιτυχημένες προσεγγίσεις στην ανάπτυξη εμβολίων λόγω των μοναδικών χαρακτηριστικών τους, όπως η αυξημένη πρόσληψή τους από τα αντιγονο-παρουσιαστικά κύτταρα, η προστασία που παρέχουν στο εγκλεισμένο αντιγόνο από μεταβολικές και απεκκριτικές διαδικασίες του οργανισμού, η χαμηλή τοξικότητά τους, καθώς και η πιθανή ανοσοδιεγερτική τους δράση. Μεταξύ αυτών, οι νανοφορείς πολυ(λακτικου-συν-γλυκολικού οξέος) (PLGA) αποτελούν την πρώτη επιλογή για τη χρήση τους ως φορείς αντιγόνων, κύριως λόγω του εξαιρετικού προφίλ τους σε ότι αφορά την βιοσυμβατότητά τους και της εγκαθιδρυμένης τους χρήσης για την ελεγχόμενη μεταφορά φαρμάκων. Σύμφωνα με τα παραπάνω, η ομάδα μας εστιάζεται στην ανάπτυξη υποψήφιων νανοεμβολίων έναντι της πειραματικής λεϊσμανίασης. Για αυτό το λόγο, σε συνεργασία με εργαστήρια χημικής μηχανικής συνθέτουμε/κατασκευάζουμε διάφορους πολυ-λειτουργικούς νανοφορείς, οι οποίοι τροποποιούνται επιλεκτικά με την ενσωμάτωση ανοσοενισχυτικών, π.χ. MPLA, CpG ODNs, για την ενίσχυση της επαγώμενης ανοσολογικής απόκρισης ή τροποποιούνται επιφανειακά για την επιτυχή στόχευση των δενδριτικών κυττάρων. Μάλιστα, τα πρώτα ενθαρρυντικά αποτελέσματα της έρευνάς μας έδειξαν ότι ο εμβολιασμός ποντικών με πολυ-λειτουργικούς PLGA νανοφορείς που εμπεριείχαν διαλυτά αντιγόνα του παρασίτου L. infantum επιφέρει σημαντική προστασία έναντι της πειραματικής σπλαχνικής λεϊσμανίασης, ανοίγοντας με αυτό τον τρόπο το δρόμο για την κατασκευή πιο εκλεπτυσμένων και ορθολογικών αντι-λεϊσμανιακών νανοεμβολίων.
Η ικανότητα του εκάστοτε εμβολίου να εγείρει τις επιθυμητές ανοσολογικές αποκρίσεις εξαρτάται όχι μόνο από το περιελαμβανόμενο αντιγόνο και ανοσοενισχυτικό, αλλά και από τις μορφολογικές ιδιότητες και το μέγεθος του ίδιου του εμβολίου. Τα τελευταία χρόνια η ανάπτυξη των νανο-εμβολίων θεωρείται μία από τις πιο επιτυχημένες προσεγγίσεις στην ανάπτυξη εμβολίων λόγω των μοναδικών χαρακτηριστικών τους, όπως η αυξημένη πρόσληψή τους από τα αντιγονο-παρουσιαστικά κύτταρα, η προστασία που παρέχουν στο εγκλεισμένο αντιγόνο από μεταβολικές και απεκκριτικές διαδικασίες του οργανισμού, η χαμηλή τοξικότητά τους, καθώς και η πιθανή ανοσοδιεγερτική τους δράση. Μεταξύ αυτών, οι νανοφορείς πολυ(λακτικου-συν-γλυκολικού οξέος) (PLGA) αποτελούν την πρώτη επιλογή για τη χρήση τους ως φορείς αντιγόνων, κύριως λόγω του εξαιρετικού προφίλ τους σε ότι αφορά την βιοσυμβατότητά τους και της εγκαθιδρυμένης τους χρήσης για την ελεγχόμενη μεταφορά φαρμάκων. Σύμφωνα με τα παραπάνω, η ομάδα μας εστιάζεται στην ανάπτυξη υποψήφιων νανοεμβολίων έναντι της πειραματικής λεϊσμανίασης. Για αυτό το λόγο, σε συνεργασία με εργαστήρια χημικής μηχανικής συνθέτουμε/κατασκευάζουμε διάφορους πολυ-λειτουργικούς νανοφορείς, οι οποίοι τροποποιούνται επιλεκτικά με την ενσωμάτωση ανοσοενισχυτικών, π.χ. MPLA, CpG ODNs, για την ενίσχυση της επαγώμενης ανοσολογικής απόκρισης ή τροποποιούνται επιφανειακά για την επιτυχή στόχευση των δενδριτικών κυττάρων. Μάλιστα, τα πρώτα ενθαρρυντικά αποτελέσματα της έρευνάς μας έδειξαν ότι ο εμβολιασμός ποντικών με πολυ-λειτουργικούς PLGA νανοφορείς που εμπεριείχαν διαλυτά αντιγόνα του παρασίτου L. infantum επιφέρει σημαντική προστασία έναντι της πειραματικής σπλαχνικής λεϊσμανίασης, ανοίγοντας με αυτό τον τρόπο το δρόμο για την κατασκευή πιο εκλεπτυσμένων και ορθολογικών αντι-λεϊσμανιακών νανοεμβολίων.
Σχετικές Δημοσιεύσεις
- Margaroni, M., M. Agallou, E. Athanasiou, O. Kammona, C. Kiparissides, C. Gaitanaki, E. Karagouni (2017). Vaccination with PLGA nanoparticles loaded with soluble Leishmania antigens and modified with a TNFα mimicking peptide or MPLA confers protection against experimental visceral leishmaniasis. International Journal of Nanomedicine (In press).
- Margaroni, M., M. Agallou, K. Kontonikola, K. Karidi, O. Kammona, C. Kiparissides, C. Gaitanaki and E. Karagouni (2016). PLGA nanoparticles modified with a TNFα mimicking peptide, soluble Leishmania antigens and MPLA induce T cell priming in vitro via dendritic cell functional differentiation. European Journal of Pharmaceutics and Biopharmaceutics 105, 18-31.
Α2. Tαυτοποίηση νέων αντιγόνων για την ανάπτυξη πεπτιδικών εμβολίων
 Τα εμβόλια που περιέχουν καθορισμένες πρωτεΐνες ή πεπτίδια υπερτερούν έναντι των κλασικών εμβολίων που περιέχουν μη-μολυσματικά ή αδρανοποιημένα παθογόνα, λόγω του ότι παράγονται εύκολα, δεν είναι μολυσματικά και μπορούν να συμπεριλάβουν μεγάλο αριθμό αντιγονικών επίτοπων στοχεύοντας με αυτό τον τρόπο σε διαφορετικά στάδια του κύκλου ζωής ή και σε διαφορετικές μορφές του παθογόνου. Προηγουμένες εργασίες της ομάδας μας έχουν δείξει ότι ο πειραματικός εμβολιασμός με δενδριτικά κύτταρα που είχαν ευαισθητοποιηθεί με αντιγονικά μόρια του παρασίτου, όπως η ιστόνη H1 ή με επιλεγμένα πεπτίδια της KMP-11, επέφεραν σημαντικά επίπεδα προστασίας στο πειραματικό μοντέλο της σπλαχνικής λεϊσμανίασης, μέσω των ειδικών CD4+ TH1 τύπου αποκρίσεων. Η ύπαρξη ασυμπτωματικών σκύλων μολυσμένων με το παράσιτο σε περιοχές που ενδημεί η σπλαχνική λεϊσμανίαση, μεταξύ των οποίων και η Ελλάδα, υποστηρίζει τη δυνατότητα ανάπτυξης ενός αποτελεσματικού εμβολίου, καθώς η παρουσία ειδικών IgG αντισωμάτων στον ορό αυτών σχετίζεται με την ύπαρξη προστατευτικής ανοσολογικής απόκρισης. Επιπλέον, η ταυτοποίηση των αντιγόνων που αναγνωρίζονται από ανοσοκυρίαρχα ειδικά αντισώματα σε αυτά τα σκυλιά θα μπορούσε να συνδράμει στην ανάπτυξη εμβολίων λόγω της σχέσης τους με το προστατευτικό προφίλ των ζώων. Με συνδυαστική εφαρμογή ανοσοπρωτεομικών και βιοπληροφορικών (in silico) προσεγγίσεων, ταυτοποιήσαμε 7 πρωτεΐνες που αναγνωρίζονται αποκλειστικά από τον ορό των ασυμπτωματικών σκύλων και χαρακτηρίζονται από υψηλή ανοσογονικότητα λόγω της συγκέντρωσης Τ κυτταρικών επίτοπων στην αλληλουχία τους έναντι των πιο συχνά απαντώμενων στον ανθρώπινο πληθυσμό HLA μορίων. Επίσης, με την εφαρμογή αποκλειστικά in silico ανάλυσης, ταυτοποιήσαμε αρκετούς επίτοπους έναντι των μορίων MHC τάξης Ι και ΙΙ προερχόμενοι από διαφορετικές πρωτεΐνες του παρασίτου Leishmania και αξιολογήσαμε την προστατευτική τους δράση στο πειραματικό μοντέλο της σπλαχνικής λεϊσμανίασης. Λαμβάνοντας υπόψη τα ενθαρρυντικά αποτελέσματα των αρχικών σχεδιασμών μας, έχουμε ξεκινήσει την in silico ανάλυση του γοδιώματος του παρασίτου Leishmania προκειμένου να ταυτοποιήσουμε νέες αντιγονικές πρωτεΐνες ή και επίτοπους για τον ορθολογικό σχεδιασμό αποτελεσματικών πεπτιδικών εμβολίων ή ακόμα και τον σχεδιασμό ευαίσθητων διαγνωστικών κιτ.
Τα εμβόλια που περιέχουν καθορισμένες πρωτεΐνες ή πεπτίδια υπερτερούν έναντι των κλασικών εμβολίων που περιέχουν μη-μολυσματικά ή αδρανοποιημένα παθογόνα, λόγω του ότι παράγονται εύκολα, δεν είναι μολυσματικά και μπορούν να συμπεριλάβουν μεγάλο αριθμό αντιγονικών επίτοπων στοχεύοντας με αυτό τον τρόπο σε διαφορετικά στάδια του κύκλου ζωής ή και σε διαφορετικές μορφές του παθογόνου. Προηγουμένες εργασίες της ομάδας μας έχουν δείξει ότι ο πειραματικός εμβολιασμός με δενδριτικά κύτταρα που είχαν ευαισθητοποιηθεί με αντιγονικά μόρια του παρασίτου, όπως η ιστόνη H1 ή με επιλεγμένα πεπτίδια της KMP-11, επέφεραν σημαντικά επίπεδα προστασίας στο πειραματικό μοντέλο της σπλαχνικής λεϊσμανίασης, μέσω των ειδικών CD4+ TH1 τύπου αποκρίσεων. Η ύπαρξη ασυμπτωματικών σκύλων μολυσμένων με το παράσιτο σε περιοχές που ενδημεί η σπλαχνική λεϊσμανίαση, μεταξύ των οποίων και η Ελλάδα, υποστηρίζει τη δυνατότητα ανάπτυξης ενός αποτελεσματικού εμβολίου, καθώς η παρουσία ειδικών IgG αντισωμάτων στον ορό αυτών σχετίζεται με την ύπαρξη προστατευτικής ανοσολογικής απόκρισης. Επιπλέον, η ταυτοποίηση των αντιγόνων που αναγνωρίζονται από ανοσοκυρίαρχα ειδικά αντισώματα σε αυτά τα σκυλιά θα μπορούσε να συνδράμει στην ανάπτυξη εμβολίων λόγω της σχέσης τους με το προστατευτικό προφίλ των ζώων. Με συνδυαστική εφαρμογή ανοσοπρωτεομικών και βιοπληροφορικών (in silico) προσεγγίσεων, ταυτοποιήσαμε 7 πρωτεΐνες που αναγνωρίζονται αποκλειστικά από τον ορό των ασυμπτωματικών σκύλων και χαρακτηρίζονται από υψηλή ανοσογονικότητα λόγω της συγκέντρωσης Τ κυτταρικών επίτοπων στην αλληλουχία τους έναντι των πιο συχνά απαντώμενων στον ανθρώπινο πληθυσμό HLA μορίων. Επίσης, με την εφαρμογή αποκλειστικά in silico ανάλυσης, ταυτοποιήσαμε αρκετούς επίτοπους έναντι των μορίων MHC τάξης Ι και ΙΙ προερχόμενοι από διαφορετικές πρωτεΐνες του παρασίτου Leishmania και αξιολογήσαμε την προστατευτική τους δράση στο πειραματικό μοντέλο της σπλαχνικής λεϊσμανίασης. Λαμβάνοντας υπόψη τα ενθαρρυντικά αποτελέσματα των αρχικών σχεδιασμών μας, έχουμε ξεκινήσει την in silico ανάλυση του γοδιώματος του παρασίτου Leishmania προκειμένου να ταυτοποιήσουμε νέες αντιγονικές πρωτεΐνες ή και επίτοπους για τον ορθολογικό σχεδιασμό αποτελεσματικών πεπτιδικών εμβολίων ή ακόμα και τον σχεδιασμό ευαίσθητων διαγνωστικών κιτ.
Σχετικές Δημοσιεύσεις
- Athanasiou, E., M. Agallou, S. Tastsoglou, O. Kammona, A. Hatzigeorgiou, C. Kiparissides, E. Karagouni (2017). Chimeric peptides containing HLA class I-restricted epitopes from Leishmania infantum proteins encapsulated in PLGA nanoparticles with MPLA induce functional differentiation of dendritic cells and promote peptide-specific IFNg-producing CD8+ T cells. Frontiers in Immunology, 8:684, org/10.3389/fimmu.2017.00684.
- Agallou, M., M. Margaroni, E. Athanasiou, D.K. Toubanaki, K. Kontonikola, K. Karidi, O. Kammona, C. Kiparissides, E. Karagouni (2017). Identification of BALB/c Immune Markers Correlated with a Partial Protection to Leishmania infantum after Vaccination with a Rationally Designed Multi-epitope Cysteine Protease A Peptide-Based Nanovaccine. PLoS Neglected Tropical Diseases, 11 (1), e0005311.
- Agallou, M., E. Athanasiou, M. Samiotaki, G. Panayotou and E. Karagouni (2016). Identification of Immunoreactive Leishmania infantum Protein Antigens to Asymptomatic Dog Sera through Combined Immunoproteomics and Bioinformatics Analysis. PLoS One 11(2), e0149894.
- Agallou, M., E. Athanasiou, O. Koutsoni, E. Dotsika and E. Karagouni (2014). Experimental Validation of Multi-Epitope Peptides Including Promising MHC Class I- and II-Restricted Epitopes of Four Known Leishmania infantum Frontiers in Immunology 5:268, doi: 10.3389/fimmu.2014.00268.
- Agallou, M., D. Smirlis, K. Soteriadou and E. Karagouni (2012). Vaccination with Leishmania histone H1-pulsed dendritic cells confers protection in murine visceral leishmaniasis. Vaccine 30(34), 5086-5093.
Agallou, M., M. Margaroni and E. Karagouni (2011). Cellular vaccination with bone marrow-derived dendritic cells pulsed with a peptide of Leishmania infantum KMP-11 and CpG oligonucleotide induces protection in a murine model of visceral leishmaniasis. Vaccine 29(31), 5053-506
Α3. Αλληλεπιδράση ξενιστή-παθογόνου: ανάλυση γονιδιώματος για τον προσδιορισμό βιοδεικτών που σχετίζονται με την ευαισθησία της νόσου ή την προστατευτική ανοσία του εμβολίου
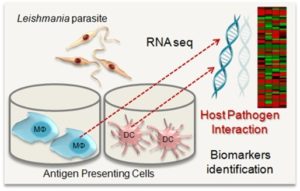 Απαραίτητη προϋπόθεση για τον σχεδιασμό νέων καθώς και τη βελτίωση των ήδη υπαρχόντων εμβολίων είναι η πληρέστερη κατανόηση των μηχανισμών που εμπλέκονται με την ανοσοαπόκριση του ξενιστή. Το πεδίο της εμβολιολογίας συστημάτων (system vaccinology) που χαρακτηρίζεται από το συνδυασμό δεδομένων που προέρχονται από την εφαρμογή μοντέρνων αναλυτικών μοριακών προσεγγίσεων και κλασικών ανοσολογικών μεθόδων, έχει ως στόχο την αποκάλυψη βιοδεικτών που σχετίζονται με την αποτελεσματικότητα των εμβολίων για τον ορθότερο σχεδιασμό και την αξιολόγησή τους. Η ομάδα μας με την εφαρμογή σύγχρονων μοριακών προσεγγίσεων (RNA-seq, μικροσυστοιχίες) στοχεύει στην αποκάλυψη αλλαγών του μεταγραφώματος που συνδέονται με την ανοσολογική απόκριση του ξενιστή έναντι του παρασίτου Leishmania με τη χρήση in vitro και in vivo μοντέλων πειραματικής μόλυνσης. Έως τώρα με την ανάλυση του μεταγραφώματος δενδριτικών κυττάρων που είχαν εκτεθεί ex vivo σε διαφορετικά νανοεμβόλια κατορθώσαμε να ταυτοποίησουμε αρκετά μόρια που μπορούν να χρησιμοποιηθούν ως δείκτες αποτελεσματικότητας ενός εμβολίου. Επίσης, προσπαθούμε να αποσαφηνίσουμε το προφίλ της ανοσολογικής απόκρισης που σχετίζεται με την ανοσοπαθολογία του σπλήνα στο πειραματικό μοντέλο της σπλαχνικής λεϊσμανίασης χρησιμοποιώντας μολυσμένα ποντίκια που έχουν εμβολιασθεί με ένα πειραματικό εμβόλιο ως συγκριτικό μοντέλο, ενώ παράλληλα διέξαγουμε ταυτόχρονη ανάλυση του μεταγραφώματος τόσο του ξενιστή όσο και του παθογόνου (dual RNA-seq) για την κατανόηση της αλληλεπίδρασης τους in vitro, χρησιμοποιώντας μολυσμένα δενδριτικά κύτταρα. Με αυτό τον τρόπο, στοχεύουμε στην ταυτοποίηση τόσο έμφυτων όσο και μεσολαβούμενων από τη μόλυνση διαταραχών στο γονιδίωμα του ξενιστή που καθορίζουν την ανοσολογική απόκριση και κατ’επέκταση στον καθορισμό βιοδεικτών για την πρόβλεψη της απόκρισης του ξενιστή στα υποψήφια εμβόλια ή/και μορίων που μπορούν να χρησιμοποιηθούν στην ανάπτυξη αποτελεσματικότερων εμβολίων.
Απαραίτητη προϋπόθεση για τον σχεδιασμό νέων καθώς και τη βελτίωση των ήδη υπαρχόντων εμβολίων είναι η πληρέστερη κατανόηση των μηχανισμών που εμπλέκονται με την ανοσοαπόκριση του ξενιστή. Το πεδίο της εμβολιολογίας συστημάτων (system vaccinology) που χαρακτηρίζεται από το συνδυασμό δεδομένων που προέρχονται από την εφαρμογή μοντέρνων αναλυτικών μοριακών προσεγγίσεων και κλασικών ανοσολογικών μεθόδων, έχει ως στόχο την αποκάλυψη βιοδεικτών που σχετίζονται με την αποτελεσματικότητα των εμβολίων για τον ορθότερο σχεδιασμό και την αξιολόγησή τους. Η ομάδα μας με την εφαρμογή σύγχρονων μοριακών προσεγγίσεων (RNA-seq, μικροσυστοιχίες) στοχεύει στην αποκάλυψη αλλαγών του μεταγραφώματος που συνδέονται με την ανοσολογική απόκριση του ξενιστή έναντι του παρασίτου Leishmania με τη χρήση in vitro και in vivo μοντέλων πειραματικής μόλυνσης. Έως τώρα με την ανάλυση του μεταγραφώματος δενδριτικών κυττάρων που είχαν εκτεθεί ex vivo σε διαφορετικά νανοεμβόλια κατορθώσαμε να ταυτοποίησουμε αρκετά μόρια που μπορούν να χρησιμοποιηθούν ως δείκτες αποτελεσματικότητας ενός εμβολίου. Επίσης, προσπαθούμε να αποσαφηνίσουμε το προφίλ της ανοσολογικής απόκρισης που σχετίζεται με την ανοσοπαθολογία του σπλήνα στο πειραματικό μοντέλο της σπλαχνικής λεϊσμανίασης χρησιμοποιώντας μολυσμένα ποντίκια που έχουν εμβολιασθεί με ένα πειραματικό εμβόλιο ως συγκριτικό μοντέλο, ενώ παράλληλα διέξαγουμε ταυτόχρονη ανάλυση του μεταγραφώματος τόσο του ξενιστή όσο και του παθογόνου (dual RNA-seq) για την κατανόηση της αλληλεπίδρασης τους in vitro, χρησιμοποιώντας μολυσμένα δενδριτικά κύτταρα. Με αυτό τον τρόπο, στοχεύουμε στην ταυτοποίηση τόσο έμφυτων όσο και μεσολαβούμενων από τη μόλυνση διαταραχών στο γονιδίωμα του ξενιστή που καθορίζουν την ανοσολογική απόκριση και κατ’επέκταση στον καθορισμό βιοδεικτών για την πρόβλεψη της απόκρισης του ξενιστή στα υποψήφια εμβόλια ή/και μορίων που μπορούν να χρησιμοποιηθούν στην ανάπτυξη αποτελεσματικότερων εμβολίων.
Σχετικές Δημοσιεύσεις
- Athanasiou, E., M. Agallou, S. Tastsoglou, O. Kammona, A. Hatzigeorgiou, C. Kiparissides, E. Karagouni (2017). Chimeric peptides containing HLA class I-restricted epitopes from Leishmania infantum proteins encapsulated in PLGA nanoparticles with MPLA induce functional differentiation of dendritic cells and promote peptide-specific IFNg-producing CD8+ T cells. Frontiers in Immunology, 8:684, org/10.3389/fimmu.2017.00684.
B. Ανάπτυξη Καινοτόμων Διαγνωστικών Χαμηλού Κόστους με Έμφαση στα Λοιμώδη Νοσήματα
Under Construction
Γ. Ανοσολογία ιχθύων / αξιολόγηση εναλλακτικών θεραπειών
 Η κατανόηση της παθολογίας των μολυσματικών ασθενειών που πλήττουν την υδατοκαλλιέργεια έχει υψηλή προτεραιότητα, καθώς η υδατοκαλλιέργεια αποτελεί σημαντικό τομέα της ελληνικής και ευρωπαϊκής οικονομίας. Φυτικά ή βακτηριακά εκχυλίσματα χρησιμοποιούνται ως συμπληρώματα διατροφής για την ενίσχυση της ανάπτυξης των ιχθύων ή εναλλακτικά μπορούν να χρησιμοποιηθούν ως αντιμικροβιακοί παράγοντες, δεδομένου ότι δεν υπάρχουν παρασιτοκτόνα χημικής προέλευσης, ενώ η χρήση αντιβιoτικών έχει αρνητική επίπτωση στην ποιότητα των ιχθύων ως τρόφιμα και στο υδάτινο περιβάλλον. Στο πλαίσιο ερευνητικών κοινοπραξιών με ακαδημαϊκά ιδρύματα και ιχθυοκαλλιεργητές, μας ενδιαφέρει: (i) να χαρακτηρίσουμε τις ανοσολογικές αποκρίσεις που εγείρονται σε φυσικές ή πειραματικά προκαλούμενες παρασιτικές ασθένειες ιχθύων με εμπορικό ενδιαφέρον για τη μεσογειακή υδατοκαλλιέργεια, (ii) να καθορίσουμε συγκεκριμένους βιοδείκτες με προγνωστική αξία και (iii) να αξιολογήσουμε εναλλακτικές θεραπείες έναντι των πιο κοινών παρασίτων των ιχθύων. Σύμφωνα με πρόσφατα αποτελέσματά μας, η μόλυνση λαβρακιών με b-nodavirus που ευθύνεται για την ιική εγκεφαλοπάθεια και αμφιβληστροειδοπάθεια, οδηγεί στην υπερέκφραση διαφόρων γονιδίων που σχετίζονται με την έμφυτη και προσαρμοστική ανοσία των ιχθύων, ενώ ιχθύες που διατράφηκαν με ιχθυοτροφή εμπλουτισμένη με αιθέριο έλαιο ρίγανης φαίνεται να είναι πιο ανθεκτικοί στη μόλυνση. Επιπλέον, έχουμε αναπτύξει μοριακές και κυτταρικές μεθόδους για τη διάγνωση και τη μαζική παραγωγή του ιού.
Η κατανόηση της παθολογίας των μολυσματικών ασθενειών που πλήττουν την υδατοκαλλιέργεια έχει υψηλή προτεραιότητα, καθώς η υδατοκαλλιέργεια αποτελεί σημαντικό τομέα της ελληνικής και ευρωπαϊκής οικονομίας. Φυτικά ή βακτηριακά εκχυλίσματα χρησιμοποιούνται ως συμπληρώματα διατροφής για την ενίσχυση της ανάπτυξης των ιχθύων ή εναλλακτικά μπορούν να χρησιμοποιηθούν ως αντιμικροβιακοί παράγοντες, δεδομένου ότι δεν υπάρχουν παρασιτοκτόνα χημικής προέλευσης, ενώ η χρήση αντιβιoτικών έχει αρνητική επίπτωση στην ποιότητα των ιχθύων ως τρόφιμα και στο υδάτινο περιβάλλον. Στο πλαίσιο ερευνητικών κοινοπραξιών με ακαδημαϊκά ιδρύματα και ιχθυοκαλλιεργητές, μας ενδιαφέρει: (i) να χαρακτηρίσουμε τις ανοσολογικές αποκρίσεις που εγείρονται σε φυσικές ή πειραματικά προκαλούμενες παρασιτικές ασθένειες ιχθύων με εμπορικό ενδιαφέρον για τη μεσογειακή υδατοκαλλιέργεια, (ii) να καθορίσουμε συγκεκριμένους βιοδείκτες με προγνωστική αξία και (iii) να αξιολογήσουμε εναλλακτικές θεραπείες έναντι των πιο κοινών παρασίτων των ιχθύων. Σύμφωνα με πρόσφατα αποτελέσματά μας, η μόλυνση λαβρακιών με b-nodavirus που ευθύνεται για την ιική εγκεφαλοπάθεια και αμφιβληστροειδοπάθεια, οδηγεί στην υπερέκφραση διαφόρων γονιδίων που σχετίζονται με την έμφυτη και προσαρμοστική ανοσία των ιχθύων, ενώ ιχθύες που διατράφηκαν με ιχθυοτροφή εμπλουτισμένη με αιθέριο έλαιο ρίγανης φαίνεται να είναι πιο ανθεκτικοί στη μόλυνση. Επιπλέον, έχουμε αναπτύξει μοριακές και κυτταρικές μεθόδους για τη διάγνωση και τη μαζική παραγωγή του ιού.
Σχετικές Δημοσιεύσεις
- Giannenas, I., I. Karamaligas, M. Margaroni, I. Pappas, E. Mayer, P. Encarnação and E. Karagouni (2015). Effect of dietary incorporation of a multi-strain probiotic on growth performance and health status in rainbow trout (Oncorhynchus mykiss). Fish Physiology & Biochemistry 41(1), 119-28.
- Rigos, G., E. Karagouni, I. Kyriazis, E. Athanasiou, K. Grigorakis, E. Kotou and P. Katharios (2013). In vitro and in vivo evaluation of quinine in gilthead sea bream, Sparus aurata naturally infected with the ciliate Cryptocaryon irritans. Aquaculture 416-417, 185-91.
Giannenas, I., E. Triantafillou, S. Stavrakakis, M. Margaroni, S. Mavridis, T. Steiner and E. Karagouni (2012). Assessment of dietary supplementation with carvacrol or thymol containing feed additives on performance, intestinal microbiota and antioxidant status of rainbow trout (Oncorhynchus mykiss). Aquaculture 350-353, 26-32.
2016-2019 ΙΔΡΥΜΑ ΣΤΑΥΡΟΣ ΝΙΑΡΧΟΣ
ΑΝΑΠΤΥΞΗ ΚΑΙΝΟΤΟΜΩΝ ΒΙΟΛΟΓΙΚΩΝ ΠΡΟΪΟΝΤΩΝ ΚΑΙ ΥΠΗΡΕΣΙΩΝ ΥΓΕΙΑΣ ΓΙΑ ΛΟΙΜΩΔΗ ΚΑΙ ΝΕΥΡΟΕΚΦΥΛΙΣΤΙΚΑ ΝΟΣΗΜΑΤΑ (ΕΥ: Δρ. Ρ. Μάτσα & Δρ. Π. Μυριαγκού)
2016 ΜΕΤΑΔΙΔΑΚΤΟΡΙΚΕΣ ΥΠΟΤΡΟΦΙΕΣ ΕΙΠ
ΑΝΑΠΤΥΞΗ ΧΙΜΑΙΡΙΚΩΝ ΠΕΠΤΙΔΙΚΩΝ ΕΜΒΟΛΙΩΝ
ΕΥ: Δρ. Ε. Καραγκούνη
Μεταδιδακτορική Συνεργάτης: Δρ. E. Αθανασίου
2015-2017 GSRT / SIEMENS
ΑΝΑΠΤΥΞΗ ΤΗΣ ΤΕΧΝΟΛΟΓΙΑΣ ΑΛΛΗΛΟΥΧΙΣΗΣ ΝΕΑΣ ΓΕΝΙΑΣ ΣΤΟΧΕΥΟΝΤΑΣ ΣΤΗ ΒΕΛΤΙΣΤΟΠΟΙΗΣΗ ΤΗΣ ΔΙΑΓΝΩΣΗΣ, ΤΗΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΕΠΙΤΗΡΗΣΗΣ ΚΑΙ ΤΟΥ ΕΛΕΓΧΟΥ ΤΩΝ ΜΟΛΥΣΜΑΤΙΚΩΝ ΑΣΘΕΝΕΙΩΝ (ΕΥ: Καθ. Μ. Μανουσάκης)
2014 EMBO/RIIP
ΠΡΑΚΤΙΚΑ ΜΑΘΗΜΑΤΑ ΒΙΟΠΛΗΡΟΦΟΡΙΚΗΣ ΚΑΙ ΓΟΝΙΔΙΩΜΑΤΙΚΗΣ ΑΝΑΛΥΣΗΣ
Οργανωτές: ΕΙΠ (Δρ. Ε. Καραγκούνη & Καθ. Μ. Μανουσάκης) και PI (Dr. F. Tekaia & Dr. E. Melanitou)
2014-2016 ΥΠΟΤΡΟΦΙΕΣ ΑΡΙΣΤΕΙΑΣ IKY ΓΙΑ ΜΕΤΑΔΙΔΑΚΤΟΡΙΚΕΣ ΣΠΟΥΔΕΣ ΣΤΗΝ ΕΛΛΑΔΑ-ΠΡΟΓΡΑΜΜΑ SIEMENS
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΒΙΟΔΕΙΚΤΩΝ ΓΙΑ ΤΗΝ ΠΡΟΚΛΙΝΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΠΡΟΦΥΛΑΚΤΙΚΩΝ Η/ΚΑΙ ΘΕΡΑΠΕΥΤΙΚΩΝ ΕΜΒΟΛΙΩΝ ΚΑΤΑ ΤΗΣ ΣΠΛΑΧΝΙΚΗΣ ΛΕΪΣΜΑΝΙΑΣΗΣ
Φορέας υποδοχής: ΕΙΠ (ΕΥ: Δρ. Ε. Καραγκούνη)
Μεταδιδακτορική Συνεργάτης: Δρ. M. Aγάλλου
2012-2015 ΓΓΕΤ, ΕΤΠΑ/ΕΣΠΑ2007-2013 – Δράση “ΑΝΑΠΤΥΞΙΑΚΕΣ ΠΡΟΤΑΣΕΙΣ ΕΡΕΥΝΗΤΙΚΩΝ ΦΟΡΕΩΝ – ΚΡΗΠΙΣ”
ΛΟΙΜΩΔΗ ΚΑΙ ΝΕΥΡΟΕΚΦΥΛΙΣΤΙΚΑ ΝΟΣΗΜΑΤΑ ΣΤΟΝ 21ο ΑΙΩΝΑ: ΑΠΟ ΤΗ ΜΕΛΕΤΗ ΤΩΝ ΒΑΣΙΚΩΝ ΜΗΧΑΝΙΣΜΩΝ ΣΤΗΝ ΑΝΑΠΤΥΞΗ ΜΕΤΑΦΡΑΣΤΙΚΗΣ ΕΡΕΥΝΑΣ ΚΑΙ ΜΕΘΟΔΟΛΟΓΙΩΝ ΑΙΧΜΗΣ ΜΕ ΣΤΟΧΟ ΤΗ ΔΙΑΓΝΩΣΗ, ΤΗΝ ΠΡΟΛΗΨΗ ΚΑΙ ΤΗ ΘΕΡΑΠΕΙΑ (MIS 450498), (ΕΥ: Δρ. Ε. Καραγκούνη)
2012-2015 ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ, ΕKT/ΕΣΠΑ2007-2013 – Δράση “ΘΑΛΗΣ”
ΑΝΑΛΥΣΗ ΜΗΧΑΝΙΣΜΩΝ ΑΝΟΣΟΠΑΘΟΓΕΝΕΙΑΣ ΣΕ ΦΥΣΙΚΕΣ ΚΑΙ ΠΕΙΡΑΜΑΤΙΚΕΣ ΜΟΛΥΝΣΕΙΣ ΙΧΘΥΩΝ ΜΕ Nodavirus: ΣΗΜΑΣΙΑ ΤΗΣ ΜΟΛΥΝΣΗΣ ΣΤΗ ΔΗΜΟΣΙΑ ΥΓΕΙΑ (MIS 375267).
Συντονιστής φορέας: Παν/μιο Θεσσαλίας (ΕΥ: Καθ. Φ. Αθανασοπούλου)
Συνεργαζόμενοι φορείς: ΑΠΘ (Καθ. Μ. Παπαναστασοπούλου), ΕΙΠ-Παν/μιο Αιγαίου-ΕΛΚΕΘΕ (Δρ. Ε. Καραγκούνη)
2011-2014 ΓΓΕΤ, ΕΤΠΑ/ΕΣΠΑ2007-2013 – Δράση “ΣΥΝΕΡΓΑΣΙΑ”
ΣΥΝΘΕΣΗ ΠΟΛΥΜΕΡΙΚΩΝ ΝΑΝΟΦΟΡΕΩΝ ΓΙΑ ΣΤΟΧΕΥΜΕΝΗ ΜΕΤΑΦΟΡΑ ΑΝΤΙΓΟΝΩΝ ΣΕ ΔΕΝΔΡΙΤΙΚΑ ΚΥΤΤΑΡΑ (09ΣΥΝ-14-643).
Συντονιστής φορέας: ΕΙΠ (ΕΥ: Δρ. Ε. Καραγκούνη)
Συνεργαζόμενοι φορείς: ΕΚΕΤΑ (Καθ. Κ. Κυπαρισσίδης), PROVET AE (Δρ. Ν. Κόρμπης)
2011-2013 ΓΓΕΤ, ΕΤΠΑ/ΕΣΠΑ2007-2013 – Δράση “ΣΥΝΕΡΓΑΣΙΑ”
ΕΝΑΛΛΑΚΤΙΚΕΣ ΜΕΘΟΔΟΙ ΠΡΟΛΗΨΗΣ ΚΑΙ ΘΕΡΑΠΕΙΑΣ ΣΤΙΣ ΕΛΛΗΝΙΚΕΣ ΥΔΑΤΟΚΑΛΛΙΕΡΓΕΙΕΣ (09ΣΥΝ-24-323).
Συντονιστής φορέας: ΕΛΚΕΘΕ (ΕΥ: Δρ. Γ. Ρήγος)
Συνεργαζόμενοι φορείς: ΕΙΠ (Δρ. Ε. Καραγκούνη), ΣΕΛΟΝΤΑ ΑΕΓΕ (Ι. Ζαρκάδας), BioMar Hellenic AΕΒE (Ι. Καρακώστας)
Margaroni M., M. Agallou, A. Vasilakaki, D. Karagkouni, G. Skoufos, A.G. Hatzigeorgiou and E. Karagouni (2022). Transcriptional Profiling of Leishmania infantum Infected Dendritic Cells: Insights into the Role of Immunometabolism in Host‐Parasite Interaction. Microorganisms 10: 1271, doi.org/10.3390/microorganisms10071271. IF2020: 4.128, Q2/Microbiology
Bilalis, P., E. Karagouni and D.K. Toubanaki (2022). Peroxidase-like activity of Fe3O4 nanoparticles and Fe3O4-graphene oxide nanohybrids: Effect of the amino- and carboxyl-surface modifications on H2O2 sensing. Applied Organometallic Chemistry, accepted. ΙF2020: 4.105, Q1/Applied chemistry
Toubanaki D.K., Efstathiou A. Karagouni E. Transcriptomic Analysis of Fish Hosts Responses to Nervous Necrosis Virus. Pathogens, 11(2), 20, doi.org/10.3390/pathogens11020201 IF2020: 3.492
2022
Balaska, A., K. Polonyfi, A. Rigatou, G. Miliotis, M. Margaroni, G.L. Daikos, M. Drogari-Apiranthitou (2021). Induction of innate immune responses by KPC-producing Klebsiella pneumonia of the pandemic sequence type 258-clade I. Access Microbiology; 3(11), doi.org/10.1099/acmi.0.000275.
2021
Agallou, M., M. Margaroni, S.D. Kotsakis, E. Karagouni (2020). A canine-directed chimeric multi-epitope vaccine induced protective immune responses in BALB/c mice infected with Leishmania infantum. Vaccines (Basel); 8(3), 350. doi: 10.3390/vaccines8030350, IF2020: 4.422
Lampou, E., C. Dovas, M. Margaroni, T. Chasalevris, T., I.S. Pappas, E. Dotsika, E. Karagouni, F. Athanassopoulou, D. Katsaras, K. Bitchava (2020). Investigation of routes of entry and dispersal pattern of RGNNV in tissues of European sea bass, Dicentrarchus labrax. Journal of Fish Diseases; 43(11). doi: 10.1111/jfd.13215, IF2020: 2.767
Toubanaki, D.K., M. Margaroni, A. Prapas, E. Karagouni (2020). Development of a nanoparticle-based lateral flow strip biosensor for visual detection of whole nervous necrosis virus particles. Scientific Reports; 10, 6529. doi: 10.1038/s41598-020-63553-z, IF2020: 4.380
2020
Agallou, M., E. Athanasiou, O. Kammona, S. Tastsoglou, A.G. Hatzigeorgiou, C. Kiparissides, E. Karagouni (2019). Transcriptome analysis identifies immune markers related to visceral leishmaniasis establishment in the experimental model of BALB/c mice. Frontiers in Immunology; 10, 2749. doi: 10.3389/fimmu.2019.02749, IF2019: 5.085
Agallou, M., E. Karagouni (2019). Detection of antigen-specific T cells in spleens of vaccinated mice applying 3[H]-Thymidine incorporation assay and luminex multiple cytokine analysis technology. Bio-protocol; 9(11), e3252. doi: 10.21769/BioProtoc.3252, IF2019: -
2019
Agallou, M., E. Pantazi, E. Tsiftsaki, D.K. Toubanaki, C. Gaitanaki, D. Smirlis, E. Karagouni (2018). Induction of protective cellular immune responses against experimental visceral leishmaniasis mediated by dendritic cells pulsed with the N-terminal domain of Leishmania infantum elongation factor-2 and CpG oligodeoxynucleotides. Mol Immunol 103, 7-20.
Toubanaki D.K., E. Karagouni (2018). Towards a Dual Lateral Flow Nanobiosensor for Simultaneous Detection of Virus Genotype-Specific PCR Products. J Anal Methods Chem. 2018:7691014.
2018
Margaroni, M., M. Agallou, E. Athanasiou, O. Kammona, C. Kiparissides, C. Gaitanaki, E. Karagouni (2017). Vaccination with PLGA nanoparticles loaded with soluble Leishmaniaantigens and modified with a TNFα mimicking peptide or MPLA confers protection against experimental visceral leishmaniasis. International Journal of Nanomedicine, In press.
Athanasiou, E., M. Agallou, S. Tastsoglou, O. Kammona, A. Hatzigeorgiou, C. Kiparissides, E. Karagouni (2017). Chimeric peptides containing HLA class I-restricted epitopes from Leishmaniainfantum proteins encapsulated in PLGA nanoparticles with MPLA induce functional differentiation of dendritic cells and promote peptide-specific IFN-producing CD8+ T cells. Frontiers in Immunology 8:684, doi.org/10.3389/fimmu.2017.00684.
Agallou, M., M. Margaroni, E. Athanasiou, D.K. Toubanaki, K. Kontonikola, K. Karidi, O. Kammona, C. Kiparissides, E. Karagouni (2017). Identification of BALB/c Immune Markers Correlated with a Partial Protection to Leishmaniainfantum after Vaccination with a Rationally Designed Multi-epitope Cysteine Protease A Peptide-Based Nanovaccine. PLoS Neglected Tropical Diseases, 11 (1), e0005311.
Toubanaki, D.K. and E. Karagouni (2017).Genotype-specific real-time PCR combined with high-resolution melting analysis for rapid identification of red-spotted grouper nervous necrosis virus. Archives of Virology, doi:10.1007/s00705-017-3375-3384.
2017
Margaroni, M., M. Agallou, K. Kontonikola, K. Karidi, O. Kammona, C. Kiparissides, C. Gaitanaki and E. Karagouni (2016). PLGA nanoparticles modified with a TNFα mimicking peptide, soluble Leishmania antigens and MPLA induce T cell priming in vitro via dendritic cell functional differentiation. European journal of Pharmaceutics and Biopharmaceutics 105, 18-31.
Sklavounos, A.A., E.K. Pefkianakis, D.K. Toubanaki, G.C. Vougioukalakis, and A.C. Calokerinos (2016). A Squaraine Derivative for Cost-Effective, Quick, and Highly Sensitive Determination of Mercury and Thiols and pH Sensing. Chem Plus Chem 81, 913-916.
Toubanaki, D.K., M. Margaroni and E. Karagouni (2016). Dual Enhancement with a Nanoparticle-Based Lateral Flow Biosensor for the Determination of DNA. Analytical Letters 49 (7), 1040-1055.
Agallou, M., E. Athanasiou, M. Samiotaki, G. Panayotou and E. Karagouni (2016). Identification of Immunoreactive Leishmania infantum Protein Antigens to Asymptomatic Dog Sera through Combined Immunoproteomics and Bioinformatics Analysis. PLoS One 11(2), e0149894.
2016
Pefkianakis, E.K., T.A. Theodossiou, D.K. Toubanaki, E.Karagouni, P. Falaras, K. Papadopoulos, and G.C. Vougioukalakis (2015). A family of potent Ru (II) Photosensitizers with enhanced DNA intercalation: bimodal photokillers. Photochemistry and Photobiology 91(5), 1191-1202.
Toubanaki, D.K., M. Margaroni and E. Karagouni (2015). Development of a novel allele-specific PCR method for rapid assessment of Nervous Necrosis Virus genotypes. Current Microbiology 71, 529-539.
Giannenas, I., I. Karamaligas, M. Margaroni, I. Pappas, E. Mayer, P. Encarnação and E. Karagouni (2015). Effect of dietary incorporation of a multi-strain probiotic on growth performance and health status in rainbow trout (Oncorhynchus mykiss). Fish Physiol Biochem. 41:119–128.
2015
Agallou, M., E. Athanasiou, O. Koutsoni, E. Dotsika and E. Karagouni (2014). Experimental Validation of Multi-Epitope Peptides Including Promising MHC Class I- and II-Restricted Epitopes of Four Known Leishmania infantum Proteins. Frontiers in Immunology 10(5), 268. doi: 10.3389/fimmu.2014.00268.
Agallou, M., E. Dotsika and E. Karagouni (2014). Low CD40 Expression Levels in Leishmania infantum-Infected Bone Marrow Dendritic Cells Evoke Regulatory Responses by Down-Regulating Interleukin-12 Production: Role of ERK1/2. European Journal of Inflammation 12(2), 315-328.
Agallou, M., E. Dotsika, S. Frydas and E. Karagouni (2014). Toll-like receptor 4 promotes control of Leishmania infantum infection through inducement of leishmanicidal activity in host macrophages: role of mitogen activated kinases. Journal of Biological Regulators and Homeostatic Agents 28(1), 41-52.
2014
Karagouni, E., O. Kammona, M. Margaroni, K. Kotti, V. Karageorgiou, C. Gaitanaki and C. Kiparissides (2013). Uptake of BSA-FITC loaded PLGA Νanoparticles by Bone Marrow-Derived Dendritic Cells induce maturation but not IL-12 or IL-10 production. Nanoscience & Nanotechnology Letters 5(4), 498-504.
2013
Giannenas, I., E. Triantafillou, S. Stavrakakis, M. Margaroni, S. Mavridis, T. Steiner and E. Karagouni (2012). Assessment of dietary supplementation with carvacrol or thymol containing feed additives on performance, intestinal microbiota and antioxidant status of rainbow trout (Oncorhynchus mykiss). Aquaculture 350-353, 26-32.
Agallou, M., D. Smirlis, K. Soteriadou and E. Karagouni (2012). Vaccination with Leishmania histone H1-pulsed dendritic cells confers protection in murine visceral leishmaniasis. Vaccine 30(34), 5086-5093.
2012
Agallou, M., M. Margaroni and E. Karagouni (2011). Cellular vaccination with bone marrow-derived dendritic cells pulsed with a peptide of Leishmania infantum KMP-11 and CpG oligonucleotide induces protection in a murine model of visceral leishmaniasis. Vaccine 29(31), 5053-5064.
2011
Symeonidou I., A. Kourelis, I. Frydas, E. Karagouni, A. Anogeianaki, M. Hatzistilianou and S. Frydas (2010). Modulation of NF-kappaΒ signalling pathways by parasites. Journal of Biological Regulators & Homeostatic Agents 24(4), 471-479.
Symeonidou I., M. Hatzistilianou, E. Papadopoulos, C.I. Dovas, E. Karagouni, S. Pappa, C.N. Pantzartzi, A. Kourelis and S. Frydas (2010). Susceptibility and resistance to canine leishmaniosis is associated to polymorphisms of the canine TNF-α gene. European Journal of Inflammation 9(1), 23-29.
Symeonidou I., S. Pappa, A. Kourelis, A. Anogeianaki, I. Frydas, E. Karagouni, M. Hatzistilianou (2010). Microarray analysis of NF-kappaB signaling pathways in PBMC of mice infected by Trichinella spiralis. International Journal of Immunopathology & Pharmacology 23(3), 821-831.
Tsatchev, I., I.D. Kyriazis, S. Boutsini, E.E. Karagouni and E.Ν. Dotsika (2010). First report of canine visceral leishmaniasis in Bulgaria. Turkish Journal of Veterinary Animal Science 34(5), 465-469.
2010
Daoudaki, M., A. Diakou, S. Frydas, I. Fouzas, E. Karagouni, N. Vavatsi, and S. Haralabidis (2009). Vaccination with Trichinella spiralis antigens increase CD8+ peripheral T cells and enhancethe TH2 immune response in Leishmaniainfantum challenged mice. International Journal of Immunopathology & Pharmacology 22(1), 169-174.
Golomazou, E., F. Athanassopoulou, E. Karagouni, L. Kokkokiris (2009). The effect of seasonality on the health and growth of a newly recorded Myxobolus species infecting cultured sharpsnout seabream (Diplodus puntazzo C.). Turkish Journal of Veterinary and Animal Sciences 33(1), 1-5.
Golomazou, E., F. Athanassopoulou, E. Karagouni, P. Tsagozis, H. Tsantilas and S. Vagianou (2006). Experimental transmission of Enteromyxum leei Diamant, Lom &Dykova, 1994 in sharpsnout seabream, Diplodus puntazzo C. and the effect on some innate immune parameters. Aquaculture 260, 44-53.
Karagouni, E., F. Athanassopoulou, S. Vagianou, H. Tsantilas, and D. Karamanis (2006). Efficacy and toxicity of orally administrated anti-coccidial drug treatment on Enteromyxum leei infections in sharpsnout seabream (Diplodus puntazzo C.). Israel Journal of Aquaculture-Bamidgeh 58(3), 157-169.
Di Giannantonio, M., S. Frydas, D. Kempuraj, E. Karagouni, M. Hatzistilianou, C.M.V. Conti, W. Boucher, N. Papadopoulou, J. Donelan, J. Cao, B. Madhappan, P. Boscolo, C. Petrarca, L. Castellani, R. Quartesan, R. Doyle and F.M. Ferro (2005). Cytokines in stress. International Journal of Immunopathology & Pharmacology 18(1), 1-5.
Karagouni, E., F. Athanassopoulou, A. Lytra, C. Comis and E. Dotsika (2005). Antiparasitic and immunomodulatory effect of innovative treatments against Myxobolus sp. infection in Diplodus puntazzo. Veterinary Parasitology 134(3-4), 215-228.
Tsagozis, P., E. Karagouni and E. Dotsika (2005). Function of CD8+ T lymphocytes in a self-curing model of visceral leishmaniasis. Parasitology International 54(2), 139-146.
Karagouni, E., F. Athanassopoulou, P. Tsagozis, E. Ralli, T. Moustakareas, K. Lytra and E. Dotsika (2005). The impact of a successful anti-myxosporean treatment on the phagocyte functions of juvenile and adult Sparus aurata L. International Journal of Immunopathology & Pharmacology 18(1), 121-132.
Frydas, S., N. Papaioannou, M. Papazahariadou, M. Hatzistilianou, E. Karagouni, M. Trakatelli, G. Brellou, C. Petrarca, M.L. Castellani, P. Conti, G. Riccioni, A. Patruno and A. Grilli (2005). Inhibition of MCP-1 and MIP-2 chemokines in murine trichinellosis: effect of the anti-inflammatory compound L-mimosine. International Journal of Immunopathology & Pharmacology 18(1), 85-93.
Frydas, S., E. Karagouni, E. Papadopoulos, M. Hatzistiliannou, S. Pappas and N. Papaioannou (2004). Chemokines and their role in parasitic diseases. European Journal of Inflammation 2(2), 53-56.
Frydas, S., E. Karagouni, T. Iezzi, D. Kempuraj, C.M.V. Conti, W. Boucher, N.G. Papadopoulou, J. Donelan, B. Madhappan, R. Letourneau, G. Carratelli, A. Grilli, F. Conti, G. Riccioni, D. Tripodi, F. Meneghini, I. Stellin and G. Sabatino (2004). Human genome project and parasitic infections. European Journal of Inflammation 2(1), 1-3.
Frydas, S., E. Karagouni, M. Hatzistilianou, D. Kempuraj, S. Comani, C. Petrarca, T. Iezzi, N. Verna, P. Conti and M.L. Castellani (2004). Cytokines and allergic disorders: Revisited study. International Journal of Immunopathology & Pharmacology 17(3), 233-235.
Tsagozis, P., V. Tseveleki, L. Probert, E. Dotsika and E. Karagouni (2004). Vaccination with plasmids encoding the Leishmania major gp63 glycoprotein and CD40L results in a partial suppression of the inflammatory reaction after experimental infection. European Journal of Inflammation 2(2), 91-96.
Athanassopoulou, F., E. Karagouni, E. Dotsika, V. Ragias, J. Tavla, P. Christofilloyanis and I. Vatsos (2004). Efficacy and toxicity of orally administrated anti-coccidial drugs for innovative treatments of Myxobolus sp. infection in Puntazzo puntazzo.Diseases of Aquatic Organisms 62, 217-226.
Athanassopoulou, F., E. Karagouni, E. Dotsika, V. Ragias, J. Tavla and P. Christofilloyanis (2004). Efficacy and toxicity of orally administrated anticoccidian drugs for innovative treatments of Polysporoplasma sparis (Sitja-Bobadilla & Alvarez-Pellitero 1885) infection in Sparus aurata L. Journal of Applied Ichthyology 20, 345-354.
Tsagozis, P., E. Karagouni and E. Dotsika (2004). Dendritic cells pulsed with peptides of gp63 induce differential protection against experimental cutaneous leishmaniasis. International Journal of Immunopathology & Pharmacology 17(3), 343-352.
Papamattheou, M.G., J.G. Routsias, E.E. Karagouni, C. Sakarellos, M. Sakarellos-Daitsiotis, H.M. Moutsopoulos, A.G. Tzioufas and E.N. Dotsika (2004). T cell help is required to induce idiotypic-anti-idiotypic autoantibody network after immunization with complementary epitope 289-308aa of La/SSB autoantigen in non-autoimmune mice. Clinical & Experimental Immunology 135, 416-426.
Frydas, S., M. Hatzistilianou, E. Karagouni, B. Madhappan, N. D’Orazio, G. Riccioni, F. Conti, G. Carratelli and D. Kempuraj (2003). Chemokines and parasites. International Journal of Immunopathology & Pharmacology 16(3), 221-224.
Tsagozis, P., E. Karagouni and E. Dotsika (2003).CD8+ T cells with parasite-specific cytotoxic activity and the TC1 profile of cytokine and chemokine secretion develop in experimental visceral leishmaniasis. Parasite Immunology 25, 569-579.
2000-2009
Sideris, V., G. Papadopoulou, E. Dotsika and E. Karagouni (1999). Asymtomatic canine leishmaniasis in greater Athens area, Greece.European Journal of Epidemiology 15, 271-276.
Frydas, S., M. Reale, D. Vacalis, R.C. Barbacane, F.C. Placido, I. Cataldo, M. Gioacchino, E. Karagouni, E. Dotsika, G. Anogiannakis, A. Trakatellis and P. Conti (1999). IgG, IgG1 and IgM response in Trichinella spiralis-infected mice treated with 4-deoxypirydoxine or fed a Vitamin B6-deficient diet. Molecular & Cellular Biochemistry 194(1-2), 47-52.
Eliades, P., E. Karagouni, I. Stergiatou and K. Miras (1998). A simple method for the serodiagnosis of human hydatid disease based on a protein A/colloidal dye conjugate. Journal of Immunological Methods 218, 123-132.
Doukas, V., F. Athanasopoulou, E. Karagouni and E. Dotsika (1998). Aeromonashydrophila infection in cultured see bass, Dicentrarchus labrax L. and Puntazzo puntazzo Cuvier from the Aegean Sea. Journal of Fish Diseases 21, 317-320.
Karagouni, E., A. Chryssikopoulos, T. Mantzavinos, N. Kanakas and E. Dotsika (1998). Ιnterleukin-1 and interleukin-1 may affect the implantation rate of patients undergoing in vitro fertilization-embryo transfer. Fertility & Sterility 70, 553-559.
Papadopoulou, G., E. Karagouni and E. Dotsika (1998). ISCOMs vaccine against experimental Leishmaniasis. Vaccine 16, 885-892.
Dotsika, E., E. Karagouni, B. Sundquist, B. Morein, A. Morgan, and M. Villacres-Eriksson (1997). Ιnfluence of Quillajasaponaria triterpenoid content on the immunomodulatory capacity of Epstein-Barr virus iscoms. Scandinavian Journal of Immunology 45, 261-268.
Chryssikopoulos A., T. Μantzavinos, N. Kanakas, E. Karagouni, E. Dotsika, and P.A. Zourlas (1996). Correlation of serum and follicular fluid concentrations of placental protein 14 and CA-125 in in vitro fertilization-embryo transfer patients. Fertility & Sterility 66(4), 599-603.
Sideris, V., E. Karagouni, G. Papadopoulou, A. Garyfallou and E. Dotsika (1996). Canine visceral leishmaniasis in the great Athens area, Greece. Parasite 3, 125-130.
Frydas, S., E. Karagouni, E. Dotsika, M. Reale, R.C. Barbacane, I. Vlemmas, G. Anogianakis, A. Trakatellis, and P. Conti (1996). Generation of TNF, IFN-, IL-6, IL-4 and IL-10 in mouse serum from trichinellosis: effect of the anti-inflammatory compound 4-deoxypyridoxine (4-DPD). Immunology Letters 49, 179-184. IF: 2,526
Haralabidis, S., E. Karagouni, S. Frydas, and E. Dotsika (1995). Immunoglobulin and cytokine profile in murine secondary hydatidosis. Parasite Immunology 17, 625-630.
Karagouni, E., S. Frydas, E. Dotsika, C. Himonas, P. Conti and A. Trakatellis (1995). Inhibition of TNF- and IL-6, but not IFN-, by 4-deoxypyridoxine (4-DPD) in Trichinella-infected mouse serum. International Journal of Immunopathology & Pharmacology 8(1), 9-14.
Fridas, S., A. Trakatellis, E. Karagouni, E. Dotsika, C. Himonas and P. Conti (1994). 4-Deoxypyridoxine inhibits chronic granuloma formation induced by potassium permanganate in vivo. Molecular & Cellular Biochemistry 136, 59-63.
Karagouni, E.E., E.N. Dotsika and A. Sklavounou (1994). Alteration in peripheral blood mononuclear cell function and serum cytokines in oral lichen planus. Journal of Oral Pathology & Medicine 23, 28-35.
Haralabidis, S., S. Frydas, E. Karagouni and C. Himonas (1992). Trichinella spiralis-Ab3 (IgG, IgM, IgA), IL-6 and TNF levels in murine trichinellosis. International Journal of Immunopathology & Pharmacology 5(3), 173-183.
Karagouni, E.E. and L. Kourounakis (1991). Anti-inflammatory and immunomodulating effects of the novel agent -(2-aminoethylamino)-2-butyrothienone. 3rd communication: Effect on suppressor cells and cytokines production in normal and adjuvant arthritic rats. Arzneimittel-Forschung/Drug Research, 41(I), 6, 647-651.
Kourounakis, L., A. Gavalas, E.E. Karagouni, D. Litina and P. Kourounakis (1991). Anti-inflammatory and immunomodulating effects of the novel agent -(2-aminoethylamino)-2-butyrothienone (-ABT). 2nd communication: Inhibitory effect on rat adjuvant induced disease. Arzneimittel-Forschung/Drug Research 41(I), 5, 537-541.
Karagouni, E.E. and L. Hadjipetrou-Kourounakis (1990). Regulation of isotype immunoglobulin and interleukin production by adjuvants in vitro. Journal of Clinical & Laboratory Immunology 33, 29-39.
Karagouni, E.E. and L. Hadjipetrou-Kourounakis (1990). Regulation of isotype immunoglobulin production by adjuvants in vivo. Scandinavian Journal of Immunology 31, 745-754.
Karagouni, E.E. and L. Hadjipetrou-Kourounakis (1990). Interleukins counteract opioid agonists immunosuppression. International Journal of Neuroscience 54(1-2), 157-163.
1990-1999
Hadjipetrou-Kourounakis, L., E. Karagounis, E. Rekka and P. Kourounakis (1989). Immunosuppression by a novel analgesic-opioid agonist. Scandinavian Journal of Immunology 29, 449-458.
1989
ΔΗΜΟΣΙΕΥΣΕΙΣ ΣΕ ΕΛΛΗΝΙΚΑ ΕΠΙΣΤΗΜΟΝΙΚΑ ΠΕΡΙΟΔΙΚΑ
Γκολομάζου Ε., Ε. Καραγκούνη, Φ. Αθανασοπούλου (2004). Τα κυριότερα Μυξοσπορίδια παράσιτα των εκτρεφομένων Μεσογειακών ψαριών. Περιοδικό της Ελληνικής Κτηνιατρικής Εταιρείας 55(4), 342-352.
Αθανασοπούλου Φ., Ε. Καραγκούνη (2004). Ρικέτσιες και μικροοργανισμοί προσομοιάζοντες με ρικέτσιες (Riketsiae–likeorganisms, RLO) σε εκτρεφόμενα ψάρια. Περιοδικό της Ελληνικής Κτηνιατρικής Εταιρείας 55(2), 165-173.
ΒΙΒΛΙΑ ΚΑΙ ΚΕΦΑΛΑΙΑ ΣΕ ΒΙΒΛΙΑ
Γαϊτανάκη Κ., Καραγκούνη Ε., Παπαζαφείρη Π., Τσιτσιλώνη Ο. (2003). Εργαστηριακές Ασκήσεις Ανοσολογίας. Εθνικό & Καποδιστριακό Παν/μιο Αθηνών, Σχολή Θετικών Επιστημών, Τμήμα Βιολογίας, Τομέας Φυσιολογίας Ζώων και Ανθρώπου (σελίδες 117).
Σοφιανός Δ., Α. Μαμαλάκη, Ε. Καραγκούνη, Β. Μυριαγκού, Π. Μαρκουλάτος, Χ. Σοφατζίδη, Κ. Μοίρας (1995). Ανάπτυξη διαγνωστικού συστήματος για την ηπατίτιδα C. Στο βιβλίο «Ηπατίτιδα C» του Σ.Ι. Χατζηγιάννη, Ιατρικές εκδόσεις Π.Χ. Πασχαλίδης, σελ. 198-205.




