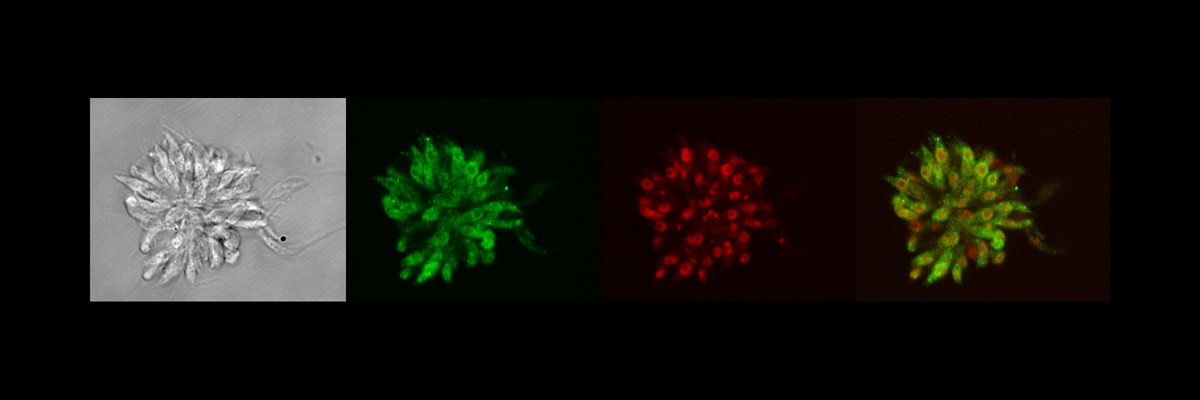

Η κύρια ερευνητική δραστηριότητα της ομάδας επικεντρώνεται στη μελέτη του πρωτοζώου της οικογένειας των Τρυπανοσωματιδών, τη Leishmania. Το παράσιτο αποτελεί αιτιολογικό παράγοντα μιας ομάδας σημαντικών παραμελημένων ασθενειών ενδημικών σε τροπικές και υποτροπικές περιοχές του πλανήτη, που χαρακτηρίζονται με τον γενικό όρο «λεϊσμανίαση». Η λεϊσμανίαση μεταδίδεται από το δήγμα της θηλυκής σκνίπας, χαρακτηρίζεται ως ανθρωποζωονόσος, ενώ κατατάσσεται μόλις δεύτερη παρασιτική νόσος μετά την ελονοσία σε έτη ζωής προσαρμοσμένα στην αναπηρία (DALYSs). Στον ξενιστή, τα παράσιτα πολλαπλασιάζονται στο λυσόσωμα των μακροφάγων αναστέλλοντας την αντιμικροβιακή δράσης τους. Μονοπάτια μεταγωγής σήματος παίζουν πολύ σημαντικό ρόλο στην αναστολή της αντιμικροβιακής δράσης των μακροφάγων και ακολούθως στην εμφάνιση και εξέλιξη της νόσου. Στον άνθρωπο η λεϊσμανίαση εμφανίζεται με διαφορετικές κλινικές εκδηλώσεις, συμπεριλαμβανομένων των δερματικών, βλεννογονοδερματικών και σπλαχνικών, με την τελευταία μορφή να είναι η πιο σοβαρή, και θανατηφόρα εάν αφεθεί χωρίς θεραπεία. Ελλείψει ενός προστατευτικού ανθρώπινου εμβολίου, ο έλεγχος της νόσου βασίζεται κυρίως στη χημειοθεραπεία, παρόλο που μόνο ελάχιστα αντιλεϊσμανιακά φάρμακα είναι διαθέσιμα, τα περισσότερα από τα οποία, παρουσιάζουν σοβαρά προβλήματα, όπως ανάπτυξη της αντιπαρασιτική αντοχή. Πέρα από το περιορισμό των αντιλεϊσμανιακών θεραπειών, μεγάλες επιδημιολογικές αλλαγές έχουν σημειωθεί στην γειτονιά μας, με την πιο σημαντική την εμφάνιση μίας νέας μονοφυλετικής ομάδας παρασίτων, που προκαλούν ανθρωπονοτική δερματική ή σπλαγχνική λεϊσμανίαση. Mε στόχο την αντιμετώπιση των τρεχουσών προκλήσεων αυτής της παραμελημένης τροπικής ασθένειας, οι βασικοί άξονες έρευνας του εργαστηρίου Μοριακής Παρασιτολογίας, περιλαμβάνουν τα ακόλουθα: (i) Μεταβίβαση σήματος και μόρια που επηρεάζουν τον κυτταρικό κύκλο, και τη μολυσματικότητα του παρασίτου Leishmania και άλλων τρυπανοσωματιδών. Σε αυτό το πλαίσιο, διαγονιδιακά παράσιτα (υπερέκφραση, knock-out/ down) και μεθοδολογίες μοριακής και κυτταρικής βιολογίας χρησιμοποιούνται για τη διερεύνηση της κυτταρικής σηματοδότησης και των σημαντικών κυτταρικών διεργασιών (κινάσες GSK3, DYRK1, Aurora). (ii) Διερεύνηση της αλληλεπίδρασης ξενιστή-παθογόνου με έμφαση στο ρόλο της μεταγωγής σήματος. Στο πλαίσιο αυτό χρησιμοποιούνται τεχνικές κυτταρικής και βιολογίας συστημάτων [ποσοτικές (φωσφο)πρωτεομικές προσεγγίσεις (συνεργασία με το Ινστιτούτο Pasteur)] για να ταυτοποιηθούν πιθανοί μοριακοί στόχοι του ξενιστή που να ενεργοποιούν την κυτταρική άμυνα του οργανισμού. iii) Έρευνα για την ανακάλυψη και ανάπτυξη καινούριων αντιλεϊσμανιακών και αντιτρυπανοσωμικών φαρμάκων. Στα πλαίσια αυτά γίνεται έλεγχος μικρών ουσιών για την αναστολή ενζύμων (ανάπτυξη μη ραδιενεργών δοκιμασιών αναστολής κινασών με ικανότητα μεσαίας σάρωσης) και την ανατολή ανάπτυξης παρασιτικών σειρών. Επιπλέον, χρησιμοποιούνται πειραματικά ζωικά μοντέλα σπλαχνικής και δερματικής λεϊσμανίασης, για τον έλεγχο της τοξικότητας και της αποτελεσματικότητας επιλεγμένων ουσιών. (iv) Κατανόηση νέων επιδημιολογικών προτύπων στην ΝΑ Ευρώπη, μηχανισμού τροπισμού και αντοχής στα φάρμακα. Διερεύνηση της σύνθετης επιδημιολογίας της Leishmania, στην περιοχή της Ανατολικής Μεσογείου (μονοφυλετική ανθρωπονοτική ομάδα παρασίτων συμπλέγματος L. donovani στην Κύπρο και L. infantum από την Κρήτη και την Κύπρο), χρησιμοποιούνται διάφορες μέθοδοι τυποποίησης και ανάλυσης όλου του γονιδιώματος.
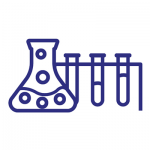
Μεταβίβαση σήματος και μόρια που επηρεάζουν τον κυτταρικό κύκλο, και τη μολυσματικότητα του παρασίτου Leishmania και άλλων τρυπανοσωματιδών
- A. Efstathiou, D. Smirlis. Leishmania Protein Kinases: Important Regulators of the Parasite Life Cycle and Molecular Targets for Treating Leishmaniasis. Microorganisms. 2021 Mar 27;9(4):691. doi: 10.3390/microorganisms9040691.
- P.C. Rocha, M. Dacher, S.A. Young, F. Kolokousi, A. Efstathiou , G.F. Späth, M.B. P. Soares, D. Smirlis. Leishmania dual-specificity tyrosine-regulated kinase 1 (DYRK1) is required for sustaining Leishmania stationary phase phenotype. Mol Microbiol. 2020 May;113(5):983-1002. doi: 10.1111/mmi.14464.
- Efstathiou A, N. Gaboriaud-Kolar, V. Myrianthopoulos, K. Vougogiannopoulou, I. Subota, S. Aicher, E. Mikros, P. Bastin, A.-L. Skaltsounis, K. Soteriadou, D. Smirlis. Indirubin Analogues Inhibit Trypanosoma brucei Glycogen Synthase Kinase 3 Short and T. brucei Growth. Antimicrob Agents Chemother. 2019 May 24;63(6):e02065-18. doi: 10.1128/AAC.02065-18.
- Alexandratos, J. Clos, M., Samiotaki, A. Efstathiou, G. Panayotou, K. Soteriadou, D. Smirlis. The loss of virulence of histone H1 over-expressing Leishmania donovani parasites is directly associated with a reduction of HSP83 rate of translation. Mol. Microbiology. 2013 Jun;88(5):1015-31.
- D. Smirlis, K. Soteriadou. Trypanosomatid apoptosis: ‘Apoptosis’ without the canonical regulators. Virulence. 2011 May 1;2(3).
- D. Smirlis, M. Duszenko, A. Jimenez-Ruiz, E. Scoulica, P. Bastien, N. Fasel, K. Soteriadou. Targeting essential pathways in trypanosomatids gives insights into protozoan mechanisms of cell death. Parasit Vectors. 2010 Nov 17;3:107. (Highly accessed).
- D. Smirlis, H. Boleti, M. Gaitanou, M. Soto, K. Soteriadou. Leishmania donovani RAN-GTPase interacts at the nuclear rim with linker histone H1. Biochem. J. 2009 Dec 10;424(3):367-74 9.
- D. Smirlis, S. Bisti, E. Xingi, G. Konidou, M. Thiakaki, K. Soteriadou. Leishmania histone H1 over-expression delays parasite cell-cycle progression, parasite differentiation and reduces Leishmania infectivity in vivo. Mol. Microbiology 2006; 60(6): 1457-73.

Διερεύνηση της αλληλεπίδρασης ξενιστή-παθογόνου με έμφαση στο ρόλο της μεταγωγής σήματος
- Smirlis, F. Dingli , V. Sabatet, A. Roth, U. Knippschild, D. Loew, G.F. Späth, N. Rachidi. Front Identification of the Host Substratome of Leishmania-Secreted Casein Kinase 1 Using a SILAC-Based Quantitative Mass Spectrometry Assay. Cell Dev Biol. 2022 Jan 3;9:800098. doi: 10.3389/fcell.2021.800098. eCollection 2021.
- Giraud, E. Rouault, L. Fiette, J.-H. Colle, D. Smirlis, E. Melanitou. Osteopontin in the host response to Leishmania amazonensis. BMC Microbiol. 2019 Feb 8;19(1):32. doi: 10.1186/s12866-019-1404-z.
- Smirlis*, F. Dingli, P. Pescher, E. Prina, D. Loew, N. Rachidi, G.F. Späth. SILAC-based quantitative proteomics reveals pleiotropic, phenotypic modulation in primary murine macrophages infected with the protozoan pathogen Leishmania donovani. Front Cell Dev Biol. 2022 Jan 3;9:800098. doi: 10.3389/fcell.2021.800098. eCollection 2021.

Έρευνα για την ανακάλυψη και ανάπτυξη καινούριων αντιλεϊμανιακών και αντιτρυπανοσωμικών φαρμάκων
- Efstathiou, D. Smirlis. A Radioactive-free Kinase I7gnhibitor Discovery Assay Against the Trypanosoma brucei Glycogen Synthase Kinase-3 short (TbGSK-3s). Bio Protoc. 2020 Jan 20;10(2):e3493. doi: 10.21769/BioProtoc.3493. eCollection 2020 Jan 20.
- Martínez de Iturrate, V. Sebastián-Pérez, M. Nácher-Vázquez, C.S. Tremper, D. Smirlis, J. Martín, A. Martínez, N.E. Campillo, L. Rivas, C. Gil. Towards discovery of new leishmanicidal scaffolds able to inhibit Leishmania GSK-3. J Enzyme Inhib Med Chem. 2020 Dec;35(1):199-210. doi: 10.1080/14756366.2019.1693704.
- Efstathiou, N. Gaboriaud-Kolar, V. Myrianthopoulos, K. Vougogiannopoulou, I. Subota, S. Aicher, E. Mikros, P. Bastin, A.-L. Skaltsounis, K. Soteriadou, D. Smirlis. Indirubin Analogues Inhibit Trypanosoma brucei Glycogen Synthase Kinase 3 Short and T. brucei Growth. Antimicrob Agents Chemother. 2019 May 24;63(6):e02065-18. doi: 10.1128/AAC.02065-18.
- Efstathiou, C.S. Meira, N. Gaboriaud-Kolar, T.M. Bastos, V.P.C. Rocha, K. Vougogiannopoulou, A.L. Skaltsounis, D. Smirlis, M.B.P. Soares. Indirubin derivatives are potent and selective anti-Trypanosoma cruzi Virulence. 2018;9(1):1658-1668. doi: 10.1080/21505594.2018.1532242. PMID: 30387370
- Smirlis & M.B.P. Soares. Selection of molecular targets for drug development against trypanosomatids. In Proteins and Proteomics of Leishmania and Trypanosoma, Springer (Editor: dos Santos, A.L.S), Subcell Biochem. 2014;74:43-76. doi: 10.1007/978-94-007-7305-9_2. (Book Chapter).
- Xingi, D. Smirlis, V. Myrianthopoulos, P. Magiatis, K. M. Grant, L. Meijer, E. Mikros, A. -L. Skaltsounis, K. Soteriadou 5-Me-6-BIO targeting the leishmanial short form affects cell-cycle progression and induces apoptosis like death: exploitation of GSK-3 for treating leishmaniasis. Int. J. Parasitol.2009;39(12):1289-303.
- Georgopoulou, D. Smirlis, S. Bisti, E. Xingi, L. Skaltsounis, K. Soteriadou. In vitro activity of 10-deacetylbaccatin-III against Leshmania donovani promastigotes and intracellular amastigotes. Planta Medica 2007 Aug;73(10):1081-8. Epub 2007 Aug 9.

Κατανόηση νέων επιδημιολογικών προτύπων στην ΝΑ Ευρώπη, μηχανισμού τροπισμού των και αντοχής στα φάρμακα
- G. Bussotti, E. Gouzelou, M. Côrtes Boité, I. Kherachi, Z. Harrat, N. Eddaikra, J.-C.Mottram, M. Antoniou, V. Christodoulou, A. Bali, F.Z. Guerfali, D. Laouini, M. Mukhtar, F. Dumetz, J.-C. Dujardin, D. Smirlis, P. Lechat, P. Pescher, A. El Hamouchi, M. Lemrani, C. Chicharro, I.P. Llanes-Acevedo, L. Botana, I. Cruz, J. Moreno, F. Jeddi, K. Aoun, A. Bouratbine, E. Cupolillo, G.F. Späth. Leishmania Genome Dynamics during Environmental Adaptation Reveal Strain-Specific Differences in Gene Copy Number Variation, Karyotype Instability, and Telomeric Amplification. mBio. 2018 Nov 6;9(6):e01399-18. doi: 10.1128/mBio.01399-18.
- Gouzelou, C. Haralambous, M. Antoniou, V. Christodoulou, F. Martinković, T. Živičnjak , D. Smirlis, F. Pratlong, J.P. Dedet, Y. Özbel, S.Ö. Toz, W. Presber, G. Schönian, K. Soteriadou. Genetic diversity and structure in Leishmania infantum populations from south eastern Europe revealed by microsatellite analysis. Parasit Vectors. 2013 Dec 5;6:342.doi: 10.1186/1756-3305-6-342. (Highly accessed).
- 2011-2012 Foundation for Education and European Culture (IPEP): “Evaluation of the anti-leishmanial action of new indirubin analogues” (2011-2012) (Main Recipient of Grant) (3000 €)
- 2011-2014 NATIONAL ACTION COOPERATION GSRT: Exploring new markers for diagnosis of resistance to antiplatelet drugs in patients with cardiovascular disease. Budget:150000€ (member)
- 2013-2015 ACIP 2013 – International Pasteur Network (IPIN): “Evaluation of Leishmania DYRK family of kinases as molecular targets for the development of anti-leishmanial drugs” (Hellenic Pasteur Institute, IP Paris, IP Montevideo, FIOCRUZ) (Coordinator) Project Budget: 59 000 €
- 2014-2015 LeiShield: A new collaborative action to determine prevalence, anticipate emergence and assess urbanization of CL and VL in LeishRIIP partner countries (PI)- (Budget 7500€)
- 2011 –2015 FP7-PEOPLE-2010-IRSES: Exploring Chemical Biodiversity with Innovative Approaches for Fighting Chagas and Leishmaniasis. PIRCES-GA-2010-269301 (Co-WP leader with Dr K. Soteriadou) Budget: 48 300 €
- 2012-2015 GSRT KRIPIS:Infectious and neurodegenerative diseases of the 21st Century: From the study of basic mechanisms to translational research and development of cutting-edge technologies aiming towards prevention, diagnosis and treatment (WP leader), Budget: 60241€ (WP Leader)
- 10-2017/ 09-2019 GSRT KRIPIS: Infectious, autoimmune and neurodegenerative diseases: Study of Pathogenic Mechanisms and development of diagnostic, prognostic and therapeutic approaches” Budget: 21000€ (WP leader)
- 2016-2017 IKY-SIEMENS: Υποτροφία μεταδιδακτορικού συνεργάρη Excellence- SIEMENS (2016-2017) supported by the Hellenic State Scholarships Foundation IKY-SIEMENS [grant no: 2016-017-0173-10398], με τίτλο “Investigation of the antiparasitic activity of drugs for the discovery of new treatments against parasitic diseases whose aetiological agents are parasites of the family of trypanosomatids” (Budget: 20 000€), 30th June 2016- 31th August 2017)
- 11/2021-8/2023 Calmette Yersin Doctoral Fellowship (Institute Pasteur Network): Phospho-signaling at the host-pathogen interface: the role of DYRKs and other kinases in Leishmania Recipient: Daniel Navarro Carrasco (33 600 euros)
2021: Internal Pasteur Grant: 5000 euros
Προσκεκλημένη Ομιλήτρια
-
- Σεμινάριο του ΕΚΠΑ (Βιολογικό) ύστερα από πρόσκληση: Η ασυνήθιστη ζωή των Τρυπανοσωματίδων. 19-12-2012
- UMR8638 CNRS-Πανεπιστήμιο Paris Descartes, “Novel drug targets and drugs for the treatment of leishmaniasis’, 19-7-2013
- Ινστιτούτο Παστέρ, Παρίσι, Επιστημονικό Συμπόσιο του Διεθνούς Δικτύου Ινστιτούτων “Exploring the role of Leishmania infantum DYRK1 and Aurora kinases in the parasitic life cycle for anti-leishmanial drug discovery”, 11-9-14
- Ινστιτούτο Παστέρ Τεχεράνης, Ιράν: International Workshop “Leishmania and leishmaniasis immunology, vaccine and drug discovery-therapy” Προσκεκλημένη εκπαιδεύτρια: “Recent approaches in anti-leishmanial drug discovery” (9/13-11-2016)
ΕΠΙΒΛΕΨΗ ΦΟΙΤΗΤΩΝ
2021-σήμερα : Daniel Carrasco Navarro, “Phospho-signalling at the host-pathogen interface: the role of DYRKs and other kinases in Leishmania infections, (Πανεπιστήμιο Alcala, Μαδρίτη, Spain;Calmette-Yersin doctoral fellowship, International Network Paris). Διδακτορική διατριβή
2023-σήμερα : Δημήτριος Κότσικος Μελέτη σηματοδοτικών μηχανισμών κατά την αλληλεπίδραση Leishmania - μακροφάγου- Διατριβή Μάστερ- Πανεπιστήμιο Δυτικής Αττικής
2022-2024 : Πίτσιας Κωνσταντίνος: Μελέτη μοριακών φαρμακευτικών στόχων του μακροφάγου για τη θεραπεία της λεϊσμανίασης. Πανεπιστήμιο Δυτικής Αττικής. Διατριβή Μάστερ
2022-2023 : Σταυρούλα Κρουστάλλη: «Επισκόπηση της αντιλεϊσμανιακής δράσης φυσικών προϊόντων» με τίτλο Βιοϊατρικές μέθοδοι, τεχνολογία στη διάγνωση, Πανεπιστήμιο Δυτικής Αττικής. Διατριβή Μάστερ
2013-2017 : Vinicius Pinto Rocha: “Leishmania infantum Dyrk1 in the development of infective promastigotes and in stage differentiation”(FIOCRUZ, Bahia, Brazil). Διδακτορική διατριβή (συνεπιβλέπουσα)
2009-2014 : Αντωνία Ευσταθίου «Μελέτη μορίων που παίζουν σημαντικό ρόλο στην ανάπτυξη των πρωτόζωων Leishmania και Trypanosoma» (ΕΚΠΑ, Σχολή Θετικών επιστημών, Τμήμα Χημείας) Διδακτορική διατριβή (συνεπιβλέπουσα)
2010-2014 : Αλέξανδρος Αλεξανδράτος, διδακτορική διατριβή “Mελέτη μορίων του πρωτοζώου Leishmania που εμπλέκονται στην πρόοδο του κυτταρικού κύκλου” (Τμήμα Χημείας, Πανεπιστημίου Ιωαννίνων) Διδακτορική διατριβή (συνεπιβλέπουσα)
1997-2001: PhD υποτροφία βραβείο της Welcome Trust Toxicology (Prize Studentship).
09/2009: Υποτροφία Συνεργασίας Σύντομης Διάρκειας, COST BM802 Life or death of protozoan parasites.
2009-2012: Αναπληρωματικό μέλος της διαχειριστικής επιτροπής- Εκπρόσωπος της Ελλάδας της δράσης COST BM0802: “Life or death of parasitic protozoa”.
4-8/2013: Υποτροφία εκπαίδευσης του προγράμματος Calmette και Yersin (International Pasteur Network) in the Molecular Parasitology and Signaling Unit of Institut Pasteur: “Generation of conditional Leishmhania Aurora null mutants for investigating the role of this kinase in the parasitic life-cycle and evaluating its potential as a putative drug target for anti-leishmanial chemotherapy”.
2013-2015: Συντονίστρια του διεθνούς προγράμματος Actions Concertées des Institus Pasteur (ACIP, 2013).
2015-2017: Αναπληρωματικό μέλος της διαχειριστικής επιτροπής- Εκπρόσωπος της Ελλάδας της δράσης COST CM1307 ACTION “Targeted chemotherapy towards diseases caused by endoparasites”“Targeted chemotherapy towards diseases caused by endoparasites”.
9-12/2015: Υποτροφία Συνεργασίας Σύντομης Διάρκειας της δράσης COST CM1307.
11-02-2016: Βραβείο από τον όμιλο Unesco-Hellas για την προσφορά στην επιστήμη.
2022
Smirlis D, Dingli F, Sabatet V, Roth A, Kippschild U, Loew D, Späth GF, Rachidi N. Identification of the Host Substratome of Leishmania-Secreted Casein Kinase 1 Using a SILAC-Based Quantitative Mass Spectrometry Assay. Front. Cell Dev. Biol., 03 January 2022
2021
Efstathiou A, Smirlis D. Leishmania Protein Kinases: Important Regulators of the Parasite Life Cycle and Molecular Targets for Treating Leishmaniasis. Microorganisms. 2021 Mar 27;9(4):691. doi: 10.3390/microorganisms9040691. (Review)
2020
Martínez de Iturrate P, Sebastián-Pérez V, Nácher-Vázquez M, Tremper CS, Smirlis D, Martín J, Martínez A, Campillo NE, Rivas L, Gil C. Towards discovery of new leishmanicidal scaffolds able to inhibit Leishmania GSK-3. J Enzyme Inhib Med Chem. 2020 Dec;35(1):199-210. doi: 10.1080/14756366.2019.1693704.
Efstathiou A and Smirlis D. A Radioactive-free Kinase Inhibitor Discovery Assay Against the Trypanosoma brucei Glycogen Synthase Kinase-3 short (TbGSK-3s). Bio-protocol, January 20, 2020; 10(02): e3493. DOI:10.21769/BioProtoc.3493. (electronic journal)
Rocha VPC, Dacher M, Young SA, Kolokousi F, Efstathiou A, Späth GF, Soares MBP, Smirlis D*. Leishmania dual-specificity tyrosine-regulated kinase 1 (DYRK1) is required for sustaining Leishmania stationary phase phenotype.Mol Microbiol. 2020 May;113(5):983-1002. doi: 10.1111/mmi.14464
Smirlis D*, Dingli F, Pescher P, Prina E, Loew D, Rachidi N, Späth GF. SILAC-based quantitative proteomics reveals pleiotropic, phenotypic modulation in primary murine macrophages infected with the protozoan pathogen Leishmania donovani. J Proteomics. 2020 Feb 20;213:103617. doi: 10.1016/j.jprot.2019.103617.
2019
Hombach-Barrigah A, Bartsch K, Smirlis D, Rosenqvist H, MacDonald A, Dingli F, Loew D, Späth .GF, Rachidi N, Wiese M, Clos J. Leishmania donovani 90 kD Heat Shock Protein - Impact of Phosphosites on Parasite Fitness, Infectivity and Casein Kinase Affinity. Sci Rep. 2019 Mar 25;9(1):5074. doi: 10.1038/s41598-019-41640-0.
Efstathiou A, Gaboriaud-Kolar N, Myrianthopoulos V, Vougogiannopoulou K, Subota I, Aicher S, Mikros E, Bastin P, Skaltsounis AL, Soteriadou K, Smirlis D. Indirubin Analogues Inhibit Trypanosoma brucei Glycogen Synthase Kinase 3 Short and T. brucei Growth. Antimicrob Agents Chemother. 2019 May 24;63(6):e02065-18. doi: 10.1128/AAC.02065-18. Print 2019 Jun.
Giraud E, Rouault E, Fiette L, Colle JH, Smirlis D, Melanitou E. Osteopontin in the host response to Leishmania amazonensis. BMC Microbiol. 2019 Feb 8;19(1):32. doi: 10.1186/s12866-019-1404-z.
2018
Bussotti G, Gouzelou E, Côrtes Boité M, Kherachi I, Harrat Z, Eddaikra N, Mottram JC, Antoniou M, Christodoulou V, Bali A, Guerfali FZ, Laouini D, Mukhtar M, Dumetz F, Dujardin JC, Smirlis D, Lechat P, Pescher P, El Hamouchi A, Lemrani M, Chicharro C, Llanes-Acevedo IP, Botana L, Cruz I, Moreno J, Jeddi F, Aoun K, Bouratbine A, Cupolillo E, Späth GF. Leishmania Genome Dynamics during Environmental Adaptation Reveal Strain-Specific Differences in Gene Copy Number Variation, Karyotype Instability, and Telomeric Amplification. mBio. 2018 Nov 6;9(6):e01399-18. doi: 10.1128/mBio.01399-18.
Agallou M, Pantazi E, Tsiftsaki E, Toubanaki DK, Gaitanaki C, Smirlis D, Karagouni E. Induction of protective cellular immune responses against experimental visceral leishmaniasis mediated by dendritic cells pulsed with the N-terminal domain of Leishmania infantum elongation factor-2 and CpG oligodeoxynucleotides. Mol Immunol. 2018 Nov;103:7-20. doi: 10.1016/j.molimm.2018.08.004.
Hombach-Barrigah A, Bartsch K, Smirlis D, Rosenqvist H, MacDonald A, Dingli F, Loew D, Späth GF, Rachidi N, Wiese M, Clos J. Leishmania donovani 90 kD Heat Shock Protein - Impact of Phosphosites on Parasite Fitness, Infectivity and Casein Kinase Affinity. Sci Rep. 2019 Mar 25;9(1):5074. doi: 10.1038/s41598-019-41640-0.
Efstathiou A, Meira CS, Gaboriaud-Kolar N, Bastos TM, Rocha VPC, Vougogiannopoulou K, Skaltsounis AL, Smirlis D, Soares MBP.Indirubin derivatives are potent and selective anti-Trypanosoma cruzi agents Virulence. 2018;9(1):1658-1668. doi:10.1080/21505594.2018.1532242.
2017
Zoidis G, Tsotinis A, Tsatsaroni A, Taylor MC, Kelly JM, Efstathiou A, Smirlis D, Fytas G. Lipophilic conformationally constrained spiro carbocyclic 2,6-diketopiperazine-1-acetohydroxamic acid analogues as trypanocidal and leishmanicidal agents: An extended SAR study. Chem Biol Drug Des. 2018 Feb;91(2):408-421. doi: 10.1111/cbdd.13088. Epub 2017 Sep 18.
Kyriazis ID, Smirlis D, Papadaki A, Koutsoni O., Aligiannis N., Skaltsounis AL, Dotsika E. Leishmanicidal Activity of Oleuropein: Leishmania donovani Promastigote Cell Death through a Possibly ROS-Independent Mechanism. J Pharmacogn Nat Prod 2017, 3:2. DOI: 10.4172/2472-0992.1000141.
2016
Azevedo L , Faqueti L., Kritsanida M., Efstathiou A., Smirlis D., Franchi Jr GC, Genta-Jouve G., Michel S., Sandjo LP, Grougnet R, Biavatti MW.Three New Trixane Glycosides Obtained From the Leaves of Jungia Sellowii Less. Using Centrifugal Partition Chromatography. Beilstein J Org Chem. 2016 Apr 12;12:674-83. doi: 10.3762/bjoc.12.68. eCollection 2016.
2015
Papadaki A, Politou AS, Smirlis D, Kotini MP, Kourou K, Papamarcaki T, Boleti HThe Leishmania Donovani Histidine Acid Ecto-Phosphatase LdMAcP: Insight Into Its Structure and Function. Biochem J. 2015 May 1;467(3):473-86. doi: 10.1042/BJ20141371.
2014
Smirlis D, Soares MB. Selection of molecular targets for drug development against trypanosomatids.. Subcell Biochem. 2014;74:43-76. doi: 10.1007/978-94-007-7305-9_2.
Stellas D, Souliotis VL, Bekyrou M, Smirlis D, Kirsch-Volders M, Degrassi F, Cundari E, Kyrtopoulos SA.Benzo[a]pyrene-induced cell cycle arrest in HepG2 cells is associated with delayed induction of mitotic instability. Mutat Res. 2014 Nov;769:59-68. doi: 10.1016/j.mrfmmm.2014.07.004. Epub 2014 Jul 19.
Efstathiou A, Gaboriaud-Kolar N, Smirlis D, Myrianthopoulos V, Vougogiannopoulou K, Alexandratos A, Kritsanida M, Mikros E, Soteriadou K, Skaltsounis AL. An inhibitor-driven study for enhancing the selectivity of indirubin derivatives towards leishmanial Glycogen Synthase Kinase-3 over leishmanial cdc2-related protein kinase 3. Parasit Vectors. 2014 May 20;7:234. doi: 10.1186/1756-3305-7-234.
Alexandratos A and Smirlis D. Protein Sample Preparation for Proteomic Analysis in Leishmania donovani. Bio-protocol . Vol 4, Iss 5, March 05, 2014. DOI: 10.21769/BioProtoc.1058.
2013
Vassilaki N, Kalliampakou KI, Kotta-Loizou I, Befani C, Liakos P, Simos G, Mentis AF, Kalliaropoulos A, Doumba PP, Smirlis D, Foka P, Bauhofer O, Poenisch M, Windisch MP, Lee ME, Koskinas J, Bartenschlager R, Mavromara P.Low oxygen tension enhances hepatitis C virus replication.J Virol. 2013 Mar;87(5):2935-48. doi: 10.1128/JVI.02534-12.
Sacconnay L, Smirlis D, Queiroz EF, Wolfender JL, Soares MB, Carrupt PA, Nurisso A.Structural insights of SIR2rp3 proteins as promising biotargets to fight against Chagas disease and leishmaniasis. Mol Biosyst. 2013 Sep;9(9):2223-30. doi: 10.1039/c3mb70180h.
Gouzelou E, Haralambous C, Antoniou M, Christodoulou V, Martinković F, Živičnjak T, Smirlis D, Pratlong F, Dedet JP, Özbel Y, Toz SÖ, Presber W, Schönian G, Soteriadou K.Genetic diversity and structure in Leishmania infantum populations from southeastern Europe revealed by microsatellite analysis. Parasit Vectors. 2013 Dec 5;6:342. doi: 10.1186/1756-3305-6-342.
Alexandratos A, Clos J, Samiotaki M, Efstathiou A, Panayotou G, Soteriadou K, Smirlis D.The loss of virulence of histone H1 overexpressing Leishmania donovani parasites is directly associated with a reduction of HSP83 rate of translation. Mol Microbiol. 2013 Jun;88(5):1015-31. doi: 10.1111/mmi.12240.
2012
Soares MB, Silva CV, Bastos TM, Guimarães ET, Figueira CP, Smirlis D, Azevedo WF Jr.Anti-Trypanosoma cruzi activity of nicotinamide. Acta Trop. 2012 May;122(2):224-9. doi: 10.1016/j.actatropica.2012.01.001.
Vassilaki N, Kalliampakou KI, Kotta-Loizou I, Befani C, Liakos P, Simos G, Mentis AF, Kalliaropoulos A, Doumba PP, Smirlis D, Foka P, Bauhofer O, Poenisch M, Windisch MP, Lee ME, Koskinas J, Bartenschlager R, Mavromara P.Low oxygen tension enhances hepatitis C virus replication.J Virol. 2013 Mar;87(5):2935-48. doi: 10.1128/JVI.02534-12.
Agallou M, Smirlis D, Soteriadou KP, Karagouni E. Vaccination with Leishmania histone H1-pulsed dendritic cells confers protection in murine visceral leishmaniasis.Vaccine. 2012 Jul 20;30(34):5086-93. doi: 10.1016/j.vaccine.2012.05.075. Epub 2012 Jun 13.
2011
Smirlis D, Soteriadou, K. Virulence. Trypanosomatid Apoptosis: 'Apoptosis' Without the Canonical Regulators. May-Jun 2011;2(3):253-6. doi: 10.4161/viru.2.3.16278. Epub 2011 May 1.DOI: 10.4161/viru.2.3.16278.
2010
Smirlis D, Duszenko M, Ruiz AJ, Scoulica E, Bastien P, Fasel N, Soteriadou K.Targeting essential pathways in trypanosomatids gives insights into protozoan mechanisms of cell death. Parasit Vectors. 2010 Nov 17;3:107. doi: 10.1186/1756-3305-3-107.
Boleti H, Smirlis D, Dalagiorgou G, Meurs EF, Christoforidis S, Mavromara P.ER targeting and retention of the HCV NS4B protein relies on the concerted action of multiple structural features including its transmembrane domains. Mol Membr Biol. 2010 Jan;27(1):45-62. doi: 10.3109/09687680903426208.
2009
Smirlis D, Boleti H, Gaitanou M, Soto M, Soteriadou K. Leishmania donovani Ran-GTPase interacts at the nuclear rim with linker histone H1. Biochem J. 2009 Dec 10;424(3):367-74. doi: 10.1042/BJ20090576.
Xingi E, Smirlis D, Myrianthopoulos V, Magiatis P, Grant KM, Meijer L, Mikros E, Skaltsounis AL, Soteriadou K. 6-Br-5methylindirubin-3'oxime (5-Me-6-BIO) targeting the leishmanial glycogen synthase kinase-3 (GSK-3) short form affects cell-cycle progression and induces apoptosis-like death: exploitation of GSK-3 for treating leishmaniasis. Int J Parasitol. 2009 Oct;39(12):1289-303. doi: 10.1016/j.ijpara.2009.04.005.
2007
Georgopoulou K, Smirlis D, Sylvia Bisti, Xingi E, Skaltsounis L, Soteriadou K. In Vitro Activity of 10-deacetylbaccatin III Against Leishmania Donovani Promastigotes and Intracellular Amastigotes. Planta Med. 2007 Aug;73(10):1081-8. doi: 10.1055/s-2007-981579.
2006
Edwards M, Wong SC, Chotpadiwetkul R, Smirlis D, Phillips IR, Shephard EA Transfection of Primary Cultures of Rat Hepatocytes. Methods Mol Biol. 2006;320:273-282. doi: 10.1385/1-59259-998-2:273.
Smirlis D, Bisti SN, Xingi E, Konidou G, Thiakaki M, Soteriadou KP. Leishmania histone H1 overexpression delays parasite cell-cycle progression, parasite differentiation and reduces Leishmania infectivity in vivo. Mol Microbiol. 2006 Jun;60(6):1457-73. doi: 10.1111/j.1365-2958.2006.05205.x.
2002
Muangmoonchai R, Wong SC, Smirlis D, Phillips IR, Shephard EA.Transfection of Liver in Vivo by Biolistic Particle Delivery: Its Use in the Investigation of Cytochrome P450 Gene Regulation.Mol Biotechnol. 2002 Feb;20(2):145-51. doi: 10.1385/mb:20:2:145
2001
Smirlis D, Muangmoonchai R, Edwards M, Phillips IR, Shephard EA. Orphan receptor promiscuity in the induction of cytochromes p450 by xenobiotics.J Biol Chem. 2001 Apr 20;276(16):12822-6. doi: 10.1074/jbc.M005930200.
Muangmoonchai R, Smirlis D, Wong SC, Edwards M, Phillips IR, Shephard EA. Xenobiotic induction of cytochrome P450 2B1 (CYP2B1) is mediated by the orphan nuclear receptor constitutive androstane receptor (CAR) and requires steroid co-activator 1 (SRC-1) and the transcription factor Sp1. Biochem J. 2001 Apr 1;355(Pt 1):71-8. doi: 10.1042/0264-6021:3550071.


